Реакция - гидрохлорирование
Cтраница 2
Установлено, что реакция гидрохлорирования 1 1 - ДХЭ в. В даиног реакционной системе большое тормозящее воздействие оказывает вода, адсорбированная стенками реакционного сосуда. Анализы показали, что содержание води в неопалес-цирукицзи растворе составляет величину 5 10 % вес. [16]
Обычно энергия активации реакции гидрохлорирования составляет 40 - 90 кДж / моль, а при низких температурах может быть равной нулю или отрицательной величиной. Ассоциация НС1 с образованием ди -, три - и тетрамеров доказана во многих работах [74-77]; ее реализации способствует низкая температура, повышенная концентрация НС1, слабополярный растворитель. [17]
Была исследована кинетика реакции гидрохлорирования ВА: образование ХП, дихлорбутена и метилвинилкетона ( рис. 6, 7) и выведено эмпирическое уравнение скорости этой реакции. [18]
Эта реакция получила название реакции гидрохлорирования и служит основой для получения многих весьма ценных химических продуктов, например хлористого этила. [19]
Каталитическое действие окисного катализатора в реакции гидрохлорирования вероятнее всего связано с тем, что хлористый водород, реагируя с окисью алюминия, образует кислоту HA1CU, которая и является собственно катализатором гидрохлорирования. [20]
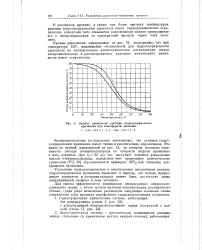 |
Кривые равновесия реакции гидрохлорирования пропилена при атмосферном давлении. [21] |
Экспериментальные исследования показывают, что реакция гидрохлорирования пропилена имеет также и кинетические ограничения. Это видно из кривой, приведенной на рис. 42, на котором показана зависимость выхода изопропилхлорида от скорости подачи пропилена в зону катализа. При г0 25 л / л час наступает заметное уменьшение выхода изопропилхлорида, вследствие чего применение кинетического уравнения ( VII, 46) ограничивается примерно 80 / 0-ной степенью превращения пропилена. [22]
Экспериментальные исследования показывают, что реакция гидрохлорирования пропилена имеет также и кинетические ограничения. Зто видно из кривой, приведенной на фиг. [23]
Экспериментальные исследования показывают, что реакция гидрохлорирования пропилена имеет также и кинетические ограничения. [24]
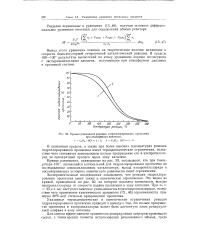 |
Кривые равновесия реакции гидрохлорирования пропилена. [25] |
Экспериментальные исследования показывают, что реакция гидрохлорирования пропилена имеет также и кинетические ограничения. Это видно из кривой, приведенной на рис. 60, на котором показана зависимость выхода изопропилхлорида от скорости подачи пропилена в зону катализа. При ио 25 л / л - час наступает заметное уменьшение выхода изопропилхлорида, вследствие чего применение кинетического уравнения ( IX, 46) ограничивается примерно 80 % - ной степенью превращения пропилена. [26]
При повышении температуры ДО0 большинства реакций гидрохлорирования принимает все более и более положительные значения. [27]
При повышении температуры Д0 большинства реакций гидрохлорирования принимает все более и более положительные значения. [28]
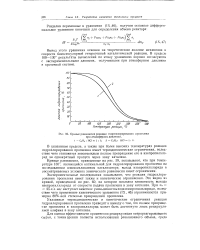 |
Кривые равновесия реакции гидрохлорирования пропилена. [29] |
Указанные термодинамические и кинетические ограничения реакции гидрохлорирования пропилена приводят к выводу о том, что полное превращение пропилена в изопропилхлорид может быть достигнуто лишь рециркуляцией олефина в зону катализа. [30]
Страницы: 1 2 3 4