Реакция - гидрохлорирование
Cтраница 3
Указанные термодинамические и кинетические ограничения реакции гидрохлорирования пропилена приводят к выводу, что полное превращение пропилена в изопропилхлорид может быть достигнуто лишь рециркуляцией олефина в зону катализа. [31]
В результате проведенных обширных исследований реакций гидрохлорирования этилена и его хлорированных производных в жидкой фазе в присутствии хлоридов железа и алюминия установлены кинетические уравнения этих процессов. Полученные экспериментальные данные позволили предложить обобщенный механизм реакций жидкофаз-ного каталитического гидрохлорирования, который дает возможность прогнозировать поведение олефинов и хлоролефинов в такого рода процессах. [32]
Указанные термодинамические и кинетические ограничения реакции гидрохлорирования пропилена приводят к выводу, что полное превращение пропилена в изопропилхлорид может быть достигнуто лишь рециркуляцией олефина в зону катализа. [33]
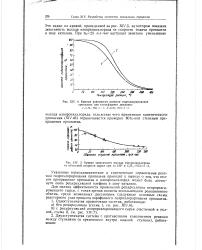 |
Кривые равновесия реакции гидрохлорирования пропилена при атмосферном давлении.| Кривая зависимости выхода изопропилхлорида от объемной скорости сырья при ( - 130 и С3НС. НС11. 2. [34] |
Указанные термодинамические и кинетические ограничения реакции гидрохлорирования пропилена приводят к выводу о том, что полное превращение пропилена в изопропилхлорид может быть достигнуто лишь рециркуляцией олефина в зону катализа. [35]
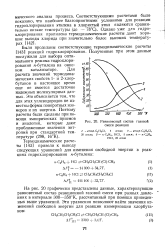 |
Равновесный состав газовой смеси реакции. [36] |
Были проделаны соответствующие термодинамические расчеты [143] реакций гидрохлорирования. Полученные при этом данные послужили для выбора оптимального режима гидрохлорирования н-бутилена на окис-ном катализаторе. Для расчета значений термодинамических свойств 1 - и 2-хлор-бутанов в настоящее время еще не имеется достаточно надежных молекулярных данных. Это объясняется тем, что для этих углеводородов не известны формы поворотных изомеров и их энергии. [37]
Есть указание [14] на возможность проведения реакции гидрохлорирования винилциклогексена в жидкой фазе с 12 N соляной кислотой при нагревании, причем отмечается, что при увеличении температуры реакции с 55 до 100 С получается преимущественно дихлорид винилциклогексена, кипящий в тех же пределах температур, что и гидрохлорид, отличающийся показателем преломления, что вызывает сомнение в правильности такого рода утверждения. Какого типа моногидрохлорид получили эти исследователи, в работе не указано. [38]
 |
Зависимость JFBX от концентрации второгэ хлэрида ( в моль. л. [39] |
Результаты опытов показывают, что скорость реакции гидрохлорирования ацетилена зависит от гидратационного числа катиона второго хлорида. Из показанных ниже данных видно, что с возрастанием гидратационного числа ( ГЧ) катиона скорость реакции повышается. [40]
Несмотря на кажущуюся простоту рассматриваемых процессов кинетика реакций гидрохлорирования изучена в немногих случаях. [41]
Исследование влияния концентрации второго хлорида на скорость реакции гидрохлорирования ацетилена показывает, что ход кривой WBX - кон - центрация второго хлорида также зависит от катиона второго хлорида. В случае хлоридов, катионы которых слабо гидратированы ( солянокислые метиламины, КС1, NH4C1), скорость реакции падает от повышения концентрации хлорида. [42]
Каталитическое действие солей ртути и меди на реакцию гидрохлорирования объясняют по-разному. Согласно одному из предложенных механизмов, сулема дает с ацетиленом продукт присоединения, называемый соединением Бигинелли. [43]
Каталитическое действие солей ртути и меди на реакцию гидрохлорирования ацетиленовых углеводородов объясняется образованием координационного комплекса ацетилен - металл, в котором происходит активация ацетилена. [44]
Смесь поступает в первый реактор, где протекает реакция гидрохлорирования ацетилена. [45]
Страницы: 1 2 3 4