Реакция - горение - углерод
Cтраница 1
Реакция горения углерода имеет первый порядок как по углероду, так и по кислороду. При низком содержании углерода, что характерно для высокотемпературной регенерации, порядок по углероду превышает первый. [1]
Реакции горения углерода являются наиболее распространенным видом гетерогенных реакций. [2]
Реакции горения углерода ( полного и неполного), окиси углерода, водорода идут с выделением тепла; это так называемые экзотермические реакции. [3]
Первичные продукты реакции горения углерода маскируются продуктами вторичных реакций. [4]
Из уравнения реакции горения углерода следует, что для сжигания 1 г-атом углерода расходуется 1 г-моль кислорода, а для сжигания 350 г-атом углерода нужно 350 г-моль кислорода. Из уравнения реакции горения водорода следует, чтодлясжигания2г - л шводорода нужно г-моль кислорода, а для сжигания 100 г-моль водорода - 50 г-моль кислорода. Выходит, для; сжигания 4200 г угле-и 200 г водорода нужно 400 г-моль ( 350 50 400) кислорода. Поскольку в было 6 25 г-моль кислорода, то нужно 393 75 г-мвль ( 400 - 6 25 393 75), или 393 75 22 4 8820 л, или 8 82 м3, кислорода. [5]
Принимаем, что реакция горения углерода протекает по первому порядку. [6]
Составьте термохимическое уравнение реакции горения углерода, если известно, что при сжигании 1 г его выделяется 33 6 кДж теплоты. [7]
 |
Теоретическое количество продуктов сгорания ( ail 0. [8] |
Для этого составляют уравнения реакции горения углерода, водорода, серы и определяют объем продуктов сгорания, приходящийся на 1 кг их. [9]
Дальнейшее развитие представлений о механизме реакций горения углерода с учетом экспериментальных исследований и структуры графита на основании открытых закономерностей процесса горения было предложено Н. В. Лавровым и рассмотрено в гл. [10]
Второй период - вначале развитие реакции горения углерода с выделением окиси углерода, которая догорает в ванне и резко повышает температуру металла. В дальнейшем происходит спад температуры ( вследствие восстановления углеродом железа из закиси железа) и в результате этого догорание кремния и марганца с выделением большого количества тепла, что приводит к горению углерода. [11]
Реакция восстановления СО2 более медленная, чем реакция горения углерода, поэтому процесс реагирования распространяется в глубь частицы угля и тем больше, чем меньше ее размер и ниже температура реагирования. Для крупных частиц углерода наблюдается уменьшение выхода окиси углерода вследствие меньшей реакционной поверхности углерода в единице объема слоя. [12]
Опытами установлено, что порядок по кислороду реакции горения углерода близок к единице. [13]
И, наоборот, зная тепловой эффект реакций горения углерода ДО СО2 и горения СО до СО2, мы легко можем подсчитать тепловой эффект реакции горения углерода до СО. [14]
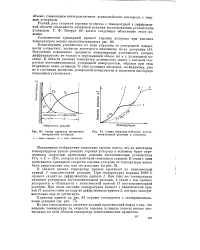 |
Схема процесса выгорания.| Схема перехода побочной восстановительной реакции в основную. [15] |
Страницы: 1 2 3