Реакция - дегалогенирование
Cтраница 1
Реакция дегалогенирования протекает медленнее, чем обычное Гидрокарбоксилирование алкинов. Однако Гидрокарбоксилирование образовавшегося дегалогенированного алкина не начинается до тех пор, пока весь галогензамещенный ацетилен не израсходуется. Очевидно, галогеналкины с атомом галогена у углеродного атома тройной связи ингибируют Гидрокарбоксилирование. [1]
Аналогично реакции дегалогенирования галогенгидринов происходит превращение [ 3-оксиалкилтолуолсульфонатов в окиси. Эта реакция находит значительное применение в области углеводов. [2]
Изучена реакция дегалогенирования л-хлоранилина на платиновых катализаторах. [3]
Аналогично реакции дегалогенирования галогенгидринов происходит превращение [ 3-оксиалкилтолуолсульфонатов в окиси. Эта реакция находит значительное применение в области углеводов. [4]
Для снижения реакции дегалогенирования предлагается восстановление галогеннитросоединений проводить при температуре ниже 150 С. Из данных таблицы видна относительная величина энергии связи хлора, брома и иода в ароматическом ядре при восстановлении галогенированных нитробензолов на никелевом катализаторе. [5]
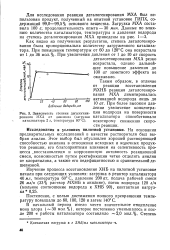 |
Зависимость степени дегалогени - ИИ водорода на поверхности. [6] |
Для исследования реакции дегалогенирования МХА был использован продукт, полученный на опытной установке ГИПХ, содержащий 99 0 - 99 5 % основного вещества. Загрузка МХА составила 100 г; продолжительность опыта - 30 мин. [7]
Для того чтобы реакция дегалогенирования шла гладко, необходимо добавить немного цинковой пыли из предыдущего опыта. [8]
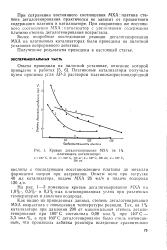 |
Кривые дегалогенирования МХА на 1 %. [9] |
Более подробные исследования реакции дегалогенирования МХА на платиновых катализаторах были проведены на пилотной установке непрерывного действия. [10]
С формальной точки зрения к реакции дегалогенирования можно отнести получение свободных четвертичны. Однако соли четвертичных аммониевых оснований - соединения хорошо диссоциированные. [11]
С большей легкостью для иодпроизводных протекает об-т ратная реакция дегалогенирования в сильнокислой среде. Так, нагревание 4 6-дииод - 1 3-дйметилбензола в концентрированной H2SO4 в течение 4 ч при 70 - 80 С приводит к 2 4 5 6-тетраиод - 1 3-диметилбензоду с выходом 75 % от теоретического. [12]
Весьма важная группа методов синтеза полифторароматиче-ских соединений заключается в реакции дегалогенирования и де-гидрогалогенирования полифтор - и полифторхлорпроизводных алициклических соединений. Последние обычно получаются при фторировании ароматических углеводородов или их хлорпроиз-водных. [13]
Следует указать, что сведений о влиянии заместителей в ядре на реакцию дегалогенирования в литературе известно очень немного. [14]
Хотя арилгалогениды, как правило, неактивны по отношению к соединениям трехвалентного фосфора, следует все же упомянуть две реакции дегалогенирования. [15]
Страницы: 1 2