Обратная реакция - окисление
Cтраница 2
 |
Принципиальная технологическая схема обезвреживания сточных вод гальванического цеха. [16] |
Последующее осаждение Cri в виде гидроокиси проводится NaOH в щелочной среде. При рН 8 происходит обратная реакция окисления Сг3 до Сг6 избытком Н2О2, поэтому Н2О2 должна удаляться из реакционной среды. [17]
 |
Принципиальная технологическая схема об врсжнвашш сточных ьид ГАДЬ-вапич1 кш о цеха. [18] |
Последующее ссаи-де-ние О1 и виде гидроокиси проводится NaOH в щслочнои среде. При рН 8 происхо ит обратная реакция окисления Сг3 до Сг избытком Н2О2, поэтому 1ЬОо должна удаляться из реакционной среды. [19]
После сжигания хлорорганических отходов образуются дымовые газы, содержащие азот, кислород, диоксид углерода, воду, хлорид водорода и незначительное количество хлора. Присутствие кислорода при охлаждении дымовых газов усиливает протекание обратной реакции окисления хлорида водорода с образованием хлора. Эта реакция ускоряется в присутствии трехвалентного оксида железа, наличие которого возможно по тракту дымовых газов из-за металлических деталей или примесей в обмуровке. Аналогичное действие оказывает и большинство минеральных солей и оксидов, присутствующих в дымовых газах. [20]
Если система находится в равновесии, то эта реакция может считаться обратной реакции окисления металлов. [21]
Уравнения (9.36) и (9.37) связывают скорость электродных реакций с величиной поляризации электрода при заметных значениях поляризации. В случае малых поляризаций суммарная скорость электродной реакции, например катодной, равна разности скоростей прямой реакции восстановления и обратной реакции окисления. [22]
Так как увеличение потенциала приводит к уменьшению ( О) и увеличению ( R), то это может происходить либо за счет увеличения скорости восстановления О, либо за счет относительного уменьшения обратной реакции окисления R до О. [23]
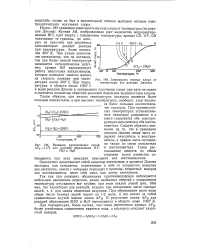 |
Зависимость выхода хлора от температуры ( по реакции Дикона. [24] |
Кривая АВ, изображающая рост количества непрореагировавшей НС1, идет кверху с повышением температуры; кривые CD, EF, GH показывают те границы, до которых на практике при различных тп Q. К - Чем лучше приготов - лен катализатор, чем он активнее, тем при более низкой температуре начинается каталитическое действие; кривая GH характеризует работу наилучших катализаторов, которые начинают заметно влиять на скорость реакции при температурах около 300 С. При температурах в области около 1000 С и выше реакция Дикона в направлении получения хлора уже идти не может и сменяется полностью обратной реакцией окисления водяного пара хлором. Таким образом, при низких температурах кислород является более сильным окислителем, а при высоких температурах, наоборот, хлор является более сильным окислителем, чем кислород. [25]
Впервые такая возможность была показана А. А. Красновским в 1948 году в опытах с хлорофиллом и восстановленной формой аскорбиновой кислоты. Интересно, что кратковременное освещение раствора хлорофилла в анаэробной среде в присутствии восстановителя приводит к образованию красной формы пигмента с максимумом поглощения 525 нм. При выключении света осуществляется обратная реакция темнового окисления фотовосстановленной ( красной) формы пигмента в нейтральную ( зеленую), причем эта темновая реакция облегчается, если в среде имеются активные окислители. [26]
Очевидно, что кислород не может окислить сложное органическое соединение непосредственно в углекислоту. В действительности дело идет о реакции декарбоксилирования - имеющиеся и образующиеся при окислении карбоксильные группы теряют углекислоту. Это объясняется тем, что кислород в процессах ассимиляции образуется не из углекислоты, а из воды. Совершенно естественно поэтому, что при обратной реакции окисления окислителем является вода, а кислороду принадлежит роль акцептора водорода. [27]
Любая стадия пути ферментативного окисления жирных кислот сама по себе обратима ( см. гл. Это позволило выдвинуть предположение, что биосинтез жирных кислот, возможно, представляет собой процесс, обратный окислительному расщеплению. Действительно, при инкубации ацетил - SKoA с очищенными окислительными ферментами, с восстановленными НАД и НАДФ и с ферментом, необратимо восстанавливающим ненасыщенные ацил - SKoA в насыщенные, происходит синтез жирных кислот. Кроме того, в ряде работ было продемонстрировано включение ацетильного остатка ацетил - SKoA в жирную кислоту в митохондриальных системах, содержавших восстановленный НАД, восстановленный НАДФ и АТФ. Теперь, однако, ясно, что существует по крайней мере два пути биосинтеза жирных кислот в митохондрии. Первый подобен процессу, происходящему в цитоплазме; это синтез жирных кислот de novo. Второй процесс состоит в удлинении цепи предобразованной жирной кислоты путем конденсации с ацетил - SKoA. Только этот второй процесс напоминает обратную реакцию окисления жирных кислот. [28]
Страницы: 1 2