Значение - потенциал - металл
Cтраница 2
Это связано с тем, что вследствие наличия на поверхности стали платины облегчается катодный процесс выделения водорода. В растворах с концентрацией ионов Pt, достаточной для пассивации, потенциал стали смещается в положительную сторону, достигая значения потенциала металла добавки. [17]
Защита стали от коррозии более эффективна, если сочетать цинковые покрытия с алюминиевыми, оловянные или хромовые покрытия на жести - с последовательно наносимыми пассивными хроматными покрытиями. В зависимости от значения потенциалов металлов основы и покрытия, с учетом их анодной или катодной поляризации и коррозионной среды, выбирают анодный или катодный способ защиты поверхности. Эти покрытия создают различными способами. [18]
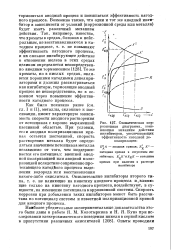 |
Схематическая коррозионная диаграмма, поясняющая механизм действия ингибиторов, увеличиванлцих эффективность катодной деполяризации. [19] |
I и II), металлы, склонные к пассивации, имеют характерную зависимость скорости анодного растворения от потенциала с хорошо выраженной пассивной областью. При условии, если анодная поляризационная кривая остается постоянной, скорость растворения металла будет определяться значением потенциала металла независимо от того, чем поддерживается его потенциал: внешней анодной поляризацией или анодной поляризацией вследствие сопряженно протекающего катодного процесса выделения водорода или восстановления какого-либо окислителя. Скорость коррозии при добавлении таких ингибиторов может быть рассчитана по потенциалу системы и известной поляризационной кривой для анодного процесса. [20]
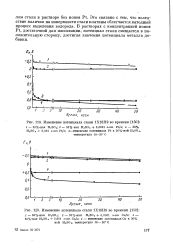
Изучена анодная поляризация Pt, Pd, Ir, Rh, Fe, Pb и Мо в растворах, содержащих 15 - 50 г / л тиокарбамида и 5 - 30 г / л серной кислоты. Измерены стационарные потенциалы металлов. Установлено, что стационарные потенциалы металлов лежат в большом диапазоне значений от - 0 27 By Pb до 0 64 В у Rh. Изменение состава электролита в различной степени оказывает влияние на значения потенциалов металлов Анализ поляризационных кривых показал, что все исследованные металлы, за исключением свинца, анодно растворяются в сернокислых растворах тиокарбамида. Установлено, что благородные металлы растворяются со значительной поляризацией. Изучена анодная поляризация Аи, Ag, Си и нержавеющей стали в растворе, содержащем 50 г / л тиоционата калия и 50 г / л карбоната калия. Установлено, что Аи, Ag и Си растворяются со значительной поляризацией. [21]
Страницы: 1 2