Многоцентровая реакция
Cтраница 1
Многоцентровая реакция состоит в объединении двух атомов одного реагента с одним или двумя атомами другого реагента, и перекрывание орбиталей между объединенными центрами сохраняется вдоль всей координаты реакции. Двухцентровые реакции включают объединение одного атома одного реагента с одним атомом другого реагента. [1]
Многоцентровые реакции требуют определенной зависимости компонента на стадии активации. Вследствие этого обычно большие отрицательные значения энтропии активации ассоциируются с небольшими величинами активационной энтальпии. [2]
Многоцентровые реакции с циклическим переносом электронов, соответствующие - присоединению и приводящие к образованию циклов, например реакции Дильса - Альдера [30] и 1 3-диполярного циклоприсоединения [31], мало зависят от полярности растворителя. Скорость 1 3-диполярного циклоприсоединения W-метил - С-фенилнитрона к этилакрилату при замене толуола на этанол понижается только примерно в шесть раз вследствие уменьшающегося в процессе активации разделения зарядов. Из этого следует, что при подобного рода циклопри-соединениях с образованием пяти - и шестичленных циклов активированный комплекс лишь незначительно отличается по своей диполярности от исходного состояния. [3]
Многоцентровые реакции требуют определенной зависимости компонента на стадии активации. Вследствие этого обычно большие отрицательные значения энтропии активации ассоциируются с небольшими величинами активационной энтальпии. [4]
 |
Возникновение перицякличесвих, антиперициклических, яеперицикличе. [5] |
Многоцентровые реакции, включающие первичное взаимодействие двух центров одного реагента с одним или двумя центрами второго реагента. В этом случае Р действует вдоль двух пар взаимодействующих центров, например пары А и пары В. [6]
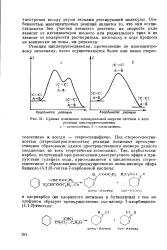 |
Кривые изменения потенциальной энергии системы в ходе реакции циклоприсоединения. [7] |
Особенностью многоцентровых реакций является то, что они осуществляются без участия внешнего реагента; их скорость мало зависит от катализаторов ионного или радикального типа и не зависит от полярности растворителя, поскольку в ходе процесса не возникают ни ионы, ни радикалы. [8]
В многоцентровых реакциях часто приписывается большое значение пространственным эффектам. Введение метпльной группы в а-положение в акриловом эфире понижает реакционную способность в 3 раза, тогда как ( 5-метильное замещение вызывает 48-кратное понижение скорости. Сравнение стирола с 1 1 - и 1 2-дифенилэтиленом приводит к выводу, что ингибирующий пространственный эффект второй фенильной группы превышает дополнительное активирующее действие, возникающее в результате расширения цепи сопряжения. Заметим в этой связи, что тетраэтилэтилентетракарб-оксилат гладко присоединяется к дифенилнитрилимину, тогда как с три - и тетраалкили-рованными или тетраарилированными олефинами реакция не идет. [9]
В многоцентровых реакциях часто приписывается большое значение пространственным эффектам. Введение метильной группы в a - цоложение в акриловом эфире понижает реакционную способность в 3 раза, тогда как ( 5-метильное замещение вызывает 48-кратное понижение скорости. Сравнение стирола с 1 1 - и 1 2-дифенилэти леном приводит к выводу, что ингибирующий пространственный эффект второй фенильной группы превышает дополнительное активирующее действие, возникающее в результате-расширения цепи сопряжения. Заметим в этой связи, что тетраэтилэтидентетракарб-оксилат гладко присоединяется к дифенилнитрилимину, тогда как с три - и тетраалкшга-рованными или тетраарилированными олефинами реакция не идет. [10]
Различные попытки интерпретации региоселективности многоцентровых реакций, какими бы успешными они ни были, основывались на оригинальной работе Фукуи [11], согласно которой предпочтительной является региохимия реакции, включающая объединение двух центров высшей граничной электронной плотности - Это справедливо для двухцентровых реакций. Однако в случае многоцентровых реакций необходимо рассмотреть вид соответствующего алгебраического выражения. Это приводит к выводу о том, что региоселективность будет наибольшей в запрещенных, шгдасно ВуАворду - Хофману, реакциях. [11]
Оно циклизуется в результате многоцентровой реакции, причем атом водорода, находящийся в орго-положении ароматического кольца, перемещается к двойной связи углерод - азот или углерод - углерод. Однако Розенталь и Гервей 677 показали, что при взаимодействии нитрилов с окисью углерода, водородом и дейтерием циклизация не сопровождается перемещением водорода к двойной связи из орго-положения. [12]
Сигматропные сдвиги относятся к типу НН-внутримолекулярных многоцентровых реакций. [13]
Те же идеи применимы к 4М - электронным многоцентровым реакциям, где стерические требования для НД - и ННД-пути значит-тельно различаются. Электроциклизации по этим соображениям исключаются. Кроме того, следует подчеркнуть, что тот же анализ справедлив, если пологая впадина на вершине термического барьера заменяется ее операционным эквивалентом - барьером с плоской вершиной. [14]
Наоборот, полярность реакции не дает основы для предсказания относительных скоростей двух изомерных многоцентровых реакций, например реакции А с А и реакции В с С, показанных ниже. [15]
Страницы: 1 2