Бимолекулярная реакция - присоединение
Cтраница 1
Бимолекулярные реакции присоединения и замещения радикалов являются реакциями развития, торможения и обрыва цепей в процессах крекинга, полимеризации и во многих других сложных превращениях органических веществ. [1]
 |
Бимолекулярные реакции обмена с участием радикалов. [2] |
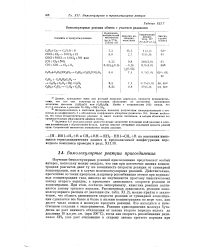
Изучение бимолекулярных реакций присоединения представляет особый интерес, поскольку можно ожидать, что они при достаточно низких концентрациях реагентов дают ту же зависимость скорости реакции от суммарной концентрации, как и в случае мономолекулярных реакций. Действительно, простейшие из таких процессов, например рекомбинация атомов при нормальных концентрациях газа, никогда не подчиняются простому кинетическому закону второго порядка, а проявляют зависимость скорости реакции от концентрации. При этом, согласно эксперименту, кинетика реакции подчиняется закону третьего порядка. Рассматривая зависимость реакции мономолекулярного распада от давления ( см. табл. XI.2), можно прийти к заключению, что область зависимости скорости реакции от суммарной концентрации сдвигается все более и более к низким концентрациям по мере того, как растет число атомов в молекуле продукта реакции. Это находится в качественном согласии с экспериментом. Реакция присоединения молекул бутадиена не дает никакого отклонения от закона второго порядка вплоть до давления 10 ммрт. [3]
К бимолекулярным реакциям присоединения относятся присоединение атома или радикала к молекуле непредельного соединения, ассоциация насыщенных молекул и некоторые другие реакции. [4]
К бимолекулярным реакциям присоединения относятся присоединение атома или радикала к молекуле непредельного соединения и ассоциация насыщенных молекул. [5]
Изложенные выше представления о механизме бимолекулярных реакций присоединения галоидов к олефинам удовлетворительно объясняют известные в настоящее время экспериментальные факты. [6]
Эти данные подтверждают возможность приближенных расчетов изменения скоростей бимолекулярных реакций присоединения в жидкой фазе с увеличением дав ления. [7]
Константа скорости роста цепи ( kp) характеризует бимолекулярную реакцию присоединения молекулы мономера к растущему полимерному радикалу, в результате которой образуется новый полимерный радикал. Константа скорости обрыва цепи ( k0) характеризует бимолекулярную реакцию между двумя растущими полимерными радикалами, в результате которой образуется одна молекула ( при рекомбинации) или две молекулы ( при диспропорционировании) неактив-ного полимера. [8]
Константа скорости роста цепи ( fep) характеризует бимолекулярную реакцию присоединения молекулы мономера к растущему полимерному радикалу, в результате которой образуется новый полимерный радикал. Константа скорости обрыва цепи ( fe0) характеризует бимолекулярную реакцию между двумя растущими полимерными радикалами, в результате которой образуется одна молекула ( при рекомбинации) или две молекулы ( при диспропорционировании) неактив-ного полимера. [9]
При переходе от бутадиена к 2-неопентжльному производному константа скорости бимолекулярной реакции присоединения к малеиновому ангидриду ( в бензоле, 25 С) возрастает примерно в 50 раз. [10]
Константа скорости роста цепи ( & р) характеризует бимолекулярную реакцию присоединения молекулы мономера к растущему полимерному радикалу, в результате которой образуется новый полимерный радикал. Константа скорости обрыва цепи ( / г0) характеризует бимолекулярную реакцию между двумя растущими полимерными радикалами, в результате которой образуется одна молекула ( при рекомбинации) или две молекулы ( при диспропорционировании) неактив-ного полимера. [11]
При переходе от бутадиена к 2-неопентильному производному константа - скорости бимолекулярной реакции присоединения к малеиновому ангидриду ( в бензоле, 25 С) возрастает примерно в 50 раз. [12]
В работе [ 933 была сделана попытка объяснить влияние структурных напряжений на кинетику бимолекулярных реакций присоединения модельных и полимерных соединений. [13]
Константа передачи цепи мономеру равна при 50 С для стирола 7 5 - 10 - 5, га-хлорстирола - 1 9 - К) - 4, о-хлорстирола - 3 0 10 - 4, а соответствующие энергии активаций равны 5 4; 5 0 и 3 5 ккал / моль. По мнению авторов, термическое зарождение радикалов происходит в результате бимолекулярной реакции присоединения. [14]
Основная причина этого состоит в следующем. В общем случае реагирующий комплекс А-В должен иметь столкновение с каким-либо третьим телом, чтобы передать ему избыток энергии и превратиться в устойчивую молекулу. Поэтому бимолекулярные реакции присоединения могут и не быть реакциями второго порядка, так как скорость их будет зависеть также от концентрации третьего вещества. [15]
Страницы: 1 2