Значение - окислительный потенциал
Cтраница 2
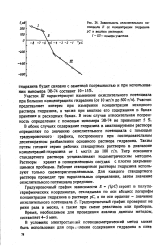 |
Зависимость окислительного потенциала В от концентрации гидразина рС в водных растворах. / - Ш - номера участков. [16] |
В обоих случаях содержание гидразина в анализируемом растворе определяют по значению окислительного потенциала с помощью градуировочного графика, построенного при последовательном десятикратном разбавлении основного раствора гидразина. Титр основного стандартного раствора устанавливают иодометрическим методом. Растворы хранят в полиэтиленовых сосудах с плотно закрывающимися пробками. Рабочие стандартные растворы гидразина используют только свежеприготовленными. Для каждого стандартного раствора проводят три параллельных определения, затем значение окислительного потенциала усредняют. [17]
Изменение состояния редоксита происходит в результате его взаимодействия с контактирующим водным раствором и отражается на значении окислительного потенциала редоксита. [18]
Опытные данные по растворимости кислорода в никеле и сплавах 79-пермаллой и 45-пермаллой в присутствии марганца представлены в табл, 1; там же приведены значения окислительного потенциала газовой фазы ( pHiO / рн), соответствующего появлению окисной фазы. [19]
Анализ теоретических положений функционирования твердых редокситов, приведенный выше, показал принципиальную возможность использования для оценки окислительно-восстановительных свойств редокс-полимеров экспериментального приема изготовления из них мембран измерительных электродов и определения значений окислительного потенциала последнего в медиаторе. [20]
Для реальных полимерных лигнинных редокс-систем представ о статической независимости отдельных окислительно-восста ельных групп не пригодно, поэтому многие приемы количеств оценки редокс-свойств к лигнинным компонентам примени Можно говорить лишь о существовании функционалы: шости между значением окислительного потенциала и содер; г групп в редокс-полимере в окисленной и восстановленной фор том их соотношения. В настоящее время значительный прогресс в химии высокомо. Они представляют собой ограничен ощие высокомолекулярные соединения трехмерной структу ] линейные), различные по составу, но содержащие групп оные вступать в обратимые окислительно-восстановительш дни с веществами, склонными к этим реакциям и находящимися такте с ними. Поскольку лигнин также относится к классу редок деров, рассмотрим теоретические предпосылки функциониров 1 твердых редокситов, содержащих общие с лигнином функционал группы, в первую очередь фенольные и хинонные. Независимо от способа синтеза, вида функциональных групп их практическое использование редоксита определяется трем лми характеристиками: значением окислительного потенциал ельной ( восстановительной) емкостью; кинетикой окисл) го-восстановительной реакции. [21]
Поскольку нормальный окислительный потенциал системы Fe / Pe44 равен - - 0 76 вольта, с практической точки зрения удобно все индикаторы разделить на две группы: на индикаторы, имеющие окислительные потенциалы больше чем 0 76 вольта, и на индикаторы, у которых значение окислительного потенциала меньше этой цифры. Представители первой группы, которых мы опишем в § 7 этой главы, часто применяются в аналитических лабораториях. [22]
Это заключение следует рассматривать как предположительное, поскольку формирование линейного участка, отвечающего этому комплексу, происходит наряду с заметной диссоциацией кислоты, которая, однако, должна увеличивать угловой коэффициент. Значения окислительного потенциала в области малых рН в этих растворах заметно больше кажущегося окислительного потенциала системы Fe ( III) - Fe ( II), равного окислительному потенциалу линейных участков с нулевым наклоном кривых зависимости ф / ( рН), отвечающих условиям С Сг и постоянства ионной силы. [23]
 |
Нормальные окислительные потенциалы некоторых пар. [24] |
MnO j - ( MnO4 - OH - e JMnO), присоединяя один электрон. Значения окислительного потенциала той и другой систем будут различны, и поэтому в реакциях нужно принимать такое значение Е0, которое соответствует протекающему процессу. [25]
Величина окислительного потенциала газовой фазы, соответствующего появлению окисной фазы, находящейся в равновесии с жидкими железом, никелем и их сплавами при 1600, уменьшается с увеличением концентрации марганца в сплаве. Значение окислительного потенциала газовой фазы для исследованных металлов и сплавов различно, и оно тем больше, чем меньше сродство металла ( сплава) к кислороду. [26]
Перуксусная кислота и кислота Каро являются сильными окислителями. В таблице 8 приведены значения окислительных потенциалов для этих кислот по сравнению с другими окислителями. Высокий окислительный потенциал позволяет использовать пероксикислоты в более мягких условиях при отбелке целлюлозы по сравнению с пероксидом водорода. [27]
 |
Окислительно-восстановительные потенциалы некоторых катализаторов, окислителей и субстратов. [28] |
При обсуждении механизма, выборе субстрата и окислителя индикаторной реакции с попеременным окислением и восстановлением катализатора оценивают принципиальную возможность ее протекания. Следует учесть, что значения реальных окислительных потенциалов определяются кислотностью растворов в соответствии с уравнением Нернста ( см. разд. Обычно каталитическую активность проявляют комплексы металлов. Комплексообразование приводит к стабилизации лигандом определенной степени окисления иона металла. [29]
Влияние авг и [ ТВг ] можно проследить с помощью уравнений линейных участков кривой зависимости ср ф ( рН) [ уравнения ( VII. Такой подход облегчает сопоставление влияния различных параметров на значение окислительного потенциала. [30]
Страницы: 1 2 3