Электролитическая реакция
Cтраница 2
Указанные выше реакции приведены здесь в качестве примеров электролитических реакций, широко используемых в синтетических целях. [16]
Появление сульфидов или элементарной серы на катоде может быть вызвано электролитическими реакциями восстановления сульфатов. [17]
 |
Ячейка с нежесткой диафрагмой. [18] |
Химически чистая ртуть ( х.ч.) может быть использована непосредственно для электролитической реакции. [19]
Теория локальных элементов, однако, не отражает полностью современные представления о механизме электролитических реакций. Количественные расчеты в рамках этой теории не обеспечивают необходимую точность из-за сложности определения суммарной поверхности всех катодных и анодных участков металла. Часто некоторые участки являются катодными в одной системе и анодными - в другой. [20]
В последующих параграфах будут рассмотрены методы, которые могут быть использованы для выяснения механизма электролитической реакции. Под механизмом реакции подразумевается последовательность отдельных стадий, которые в действительности протекают последовательно или одновременно и в совокупности образуют суммарную электродную реакцию. Выявление этой последовательности реакций, как и в химической кинетике, возможно только экспериментальным путем. Теоретическое вычисление, например на основе квантовой теории, еще невозможно. [21]
Травление представляет избирательное изменение различных составляющих структуры, происходящее большей частью благодаря химическим или электролитическим реакциям между шлифом и травнтелем. [22]
Травление представляет избирательное изменение различных составляющих структуры, происходящее большей частью благодаря химическим или электролитическим реакциям между шлифом и травителем. [23]
Травление представляет избирательное изменение различных составляющих структуры, происходящее большей частью благодаря химическим или электролитическим реакциям между шлифом и травнтелем. [24]
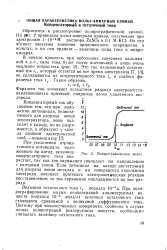 |
Полярографическая волна. [25] |
Если потенциал на катоде достаточный для разряда ионов металла и на поверхности капельного электрода начинает протекать электролитическая реакция восстановления, то ток заряжения накладывается на ток разряда. [26]
Несмотря на эти недостатки, книга в целом представляет собой ценное методическое руководство по практическому осуществлению каталитических, фотохимических и электролитических реакций и окажет существенную пользу широкому кругу химиков, исследующих или просто использующих в своей работе эти важные реакции. [27]
Появление сигнала ЭПР является доказательством образования радикал-ионов в электрохимическом процессе и тем самым дает информацию о механизме электролитической реакции. Отсутствие сигнала ЭПР не всегда исключает возможность образования радикал-ионов, но может говорить об их малой стабильности или о непригодности выбранных экспериментальных условий для детектирования радикал-ионов. [28]
Подготовка поверхности и процесс ее обработки заключаются в последовательном погружении детали в несколько ванн, в которых происходят химические или электролитические реакции. [29]
Пористая диафрагма должна оказывать как можно меньшее сопротивление диффузии неорганических ионов и как можно большее-диффузии органических соединений, участвующих в электролитической реакции. Если сосуд слишком порист и допускает слишком большие потери органических веществ, то его поры можно уменьшить, заполнив их каким-нибудь подходящим материалом. Для определения пористости сосуда его наполняют до верха водой и дают ей возможность вытечь в пустой мерный цилиндр. Если из сосуда емкостью около 150 мл вытекает воды больше, чем около 1 мл / час, то его следует подвергнуть дополнительной обработке, чтобы уменьшить размер пор. Характер обработки зависит от того, какой используют электролит-кислый или щелочной. [30]
Страницы: 1 2 3