Указанная реакция
Cтраница 4
Указанная реакция протекает однако не только с этиловым спиртом, но и с некоторыми другими спиртами, альдегидами, кетонами, кислотами и сложными эфирами, например с вторичным бутиловым спиртом СН3 - СН ( ОН) - СН2 - СН3, уксусным альдегидом СН3 - СНО, ацетоном СН3 - СО-СЙ3, обыкновенной молочной кислотой СН3 - СН ( ОН) - СООН, этиловым эфиром уксусной кислоты СН3 - СО-ОС2Н6 и др.; тем не менее вполне возможно определить независимо друг от друга например ацетон и этиловый спирт, находящиеся в одном растворе, так как образование из этих соединений йодоформа сильно зависит от рН раствора. Йодоформ получается из ацетона при значительно меньшем рН, чем из этилового спирта. [46]
Указанная реакция не является единственной реакцией, протекающей как 1 4-присоединение. [47]
Указанная реакция дает возможность произвести приблизительный подсчет энергетических затрат, необходимых для окисления фенола, и определить, насколько рационально расходуется электроэнергия. [48]
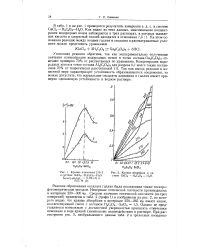 |
Кривые изменения [ Н ].| Кривые абсорбции в системе GaCl3 - Н2С2О4 - Н2О. [49] |
Указанная реакция обратима, так как экспериментально полученные значения концентрации водородных ионов в точке состава Ga2 ( C2O4) 3 отвечают примерно 70 % от рассчитанных по уравнению. Так как выход реакции в известной мере характеризует устойчивость образовавшегося соединения, то можно допустить, что нормальные оксалаты алюминия и галлия имеют примерно одинаковую устойчивость в водном растворе. [50]
Указанная реакция является примером превращения ароматического соединения в соединение жирного ряда. [51]
Указанная реакция для тетрагидрофурана протекает достаточно медленно и представляет практическую опасность при температурах выше 40 С. Однако в ряде других случаев, например при использовании метилаля, процесс эффективно идет уже при комнатной температуре. [52]
Указанные реакции (2.69) - (2.72) подтверждают предположение о том, что небольшие количества воды ( до 2 %) способствуют инициированию реакции окисления. [53]
Страницы: 1 2 3 4