Значение - произведение - растворимость
Cтраница 3
 |
Произведение растворимости некоторых труднорастворимых в воде веществ. [31] |
В табл. 5 приводятся значения произведений растворимости различных соединений. [32]
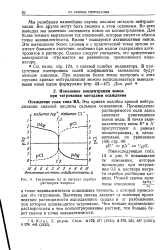 |
Титрование 0 1 н. нитрата серебра раствором хлорида. [33] |
Величина скачка зависит от значения произведения растворимости выпадающего осадка и от разбавления, при котором производится титрование. [34]
В табл. 5 приводятся значения произведений растворимости различных соединений. [35]
В табл. 40 приведены значения произведения растворимости растворимости гидроокисей катионов четвертой группы. [36]
Соответственно этому в выражении значения произведения растворимости электролита, который состоит из двух и большего числа одинаковых ионов, активность такого иона берется в степени, равной числу образующихся ионов. [37]
Если подставить в это выражение значение произведения растворимости малорастворимого сульфида двухвалентного металла, то можно рассчитать максимальную концентрацию ионов водорода, при которой соответствующий сульфид должен практически полиостью осаждаться. [38]
В той же таблице приведены значения произведений растворимости соответствующих гидроокисей и константы нестойкости тетрааммиакатов. Сопоставление этих данных показывает, что произведения растворимости оксинатов двухвалентных катионов значительно меньше произведений растворимости соответствующих гидроокисей, тогда как для трехвалентных катионов имеет место обратное отношение. Повидимому, в данном случае огромную роль играет способность двухвалентных катионов координировать атом азота; она достаточно хорошо характеризуется приведенными в таблице значениями констант нестойкости соответствующих тетраммино-комплексов. Для А13 и Fe3, как это указывает Эфраим, получить аммиакаты в водном растворе вообще невозможно. [39]
Действительно, как следует из значений произведения растворимости, концентрация ионов металла в прианодном слое должна быть минимальной в случае стального анода, вследствие чего осаждение на нем происходит за счет ионов Н, а связующее осаждается в кислой форме. [40]
Ниже дана схема расчета растворимости из значения произведения растворимости. [41]
Ниже дан пример расчета растворимости по значению произведения растворимости. [42]
Ниже дан пример расчета растворимости по значению произведения растворимости. [43]
В ранних работах было показано, что значение произведения растворимости LaF3 не совпадает с табличным ПР10 - 27 и меняется в процессе титрования вследствие старения осадка от 10 - 5 до 10 - 17 09, что является причиной дрейфа потенциала вблизи конечной точки титрования в сторону его увеличения. [44]
Иначе говоря, если произведение граммионных концентраций гвышает значение произведения растворимости, происходит ждение электролитов; если же произведение граммионных щентраций не достигает значения произведения раствори-сти, то электролит не осаждается, а при наличии твердой фазы эеходит в раствор. [45]
Страницы: 1 2 3 4