Регенерация - фермент
Cтраница 2
После окончания первого цикла гидролиза непрогидролизо-ванный остаток целлюлозы с прочно адсорбированными на нем ферментами отделяют от раствора, содержавшего слабо адсорбирующиеся ферменты и продукты гидролиза. Регенерацию ферментов из раствора осуществляют с помощью ультрафильтрации на волокнах или ацетилцеллю лозных мембранах. Полученную после этого концентрированную фракцию, содержавшую слабо адсорбирующиеся ферменты, разбавляют буфером до первоначального объема. [16]
Гены, ответственные за синтез т - РНК, необходимой для производства синтезирующих каучук ферментов, а также система, продуцирующая рибосомы, по-видимому, дерепрессируются действием подсочки, ибо и тп - РНК, и ферменты в большом количестве появляются в регенерирующем млечном соке. По мере того как в млечном сосуде происходит регенерация ферментов, связанных с синтезом каучука, а концентрация, последнего приближается к верхнему пределу, характерному для растения, активность отмеченных выше генов вновь репрессируется, а ферменты, связанные с синтезом каучука, ингиби-руются; действительно, всякий синтез в сосуде полностью прекращается. [17]
Технологическая линия получения глюкозы ферментативным путем включает как новые биотехнологические, так и известные технологические стадии. К биотехнологическим стадиям относятся получение целлюлаз, ферментативный гидролиз, регенерация ферментов, обработка гидролизата целлобиазой для увеличения выхода глюкозы. [18]
Вполне естественно было предположить, что и в нашем случае мы имеем дело именно с такими дыхательными хромогенами, поглощавшими атмосферный кислород и переходившими вследствие этого в дыхательные пигменты. Но если это так, если действительно окисление зимогена, а следовательно регенерация фермента происходит через посредство дыхательных пигментов, то стоит только очистить экстракт, удалить из раствора хромогены и пигменты, и тогда все явление регенерации должно исчезнуть. Это на самом деле и происходит в том случае, если мы осадим экстракт из ростков солода солью какого-либо тяжелого металла, например сулемой. Опыты ставились следующим образом: 10 г муки ростков солода смеши. [19]
В ходе этой реакции молекулы субстрата S взаимодействуют с фермен - TOIV: Е, образуя фермент-субстратный комплекс ES. Затем этот комплекс по второй реакции превращается в конечный продукт Р с регенерацией фермента. ES, но в данном случае в стационарных условиях концентрация ES остается практически постоянной. Таким образом, определяющую роль в кинетике играет реакция превращения ES в продукт. [20]
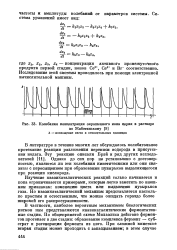 |
Колебания концентрации окрашенного иона церия в растворе. [21] |
В частности, наиболее вероятным механизмом биологических ритмов нам представляются квазикаталитические ферментативные стадии. По общепринятой схеме Михаэлиса действие ферментов протекает в две стадии: образование комплекса фермент - субстрат и регенерация фермента из него. [22]
В-третьих, боргидрид натрия, представляющий собой мягкий восстанавливающий агент, реагирующий с CN ( но не С-N), кетонной или амидной карбонильными группами, восстанавливает комплекс фермент - субстрат, полученный из меченного 14С ацетоацетата. В результате образуется продукт, не обладающий ферментативной активностью, в котором при диализе сохраняется практически все количество 14С, и регенерации фермента не происходит. Действие боргидри-да натрия на комплекс фермент - субстрат - цианистый водород с последующим диализом приводит к регенерации фермента, полностью сохранившего свою активность. [23]
Терапия отравлений эфирами фосфорной кислоты основывается уже много лет на применении атропина и аналогичных ему по действию производных. В последние годы из работ Вильсона стало известно о других новых синтетических фармацевтических средствах, которые в состоянии в известных случаях прервать блокаду холинэстеразы и привести к регенерации фермента. Однако эти вещества в настоящее время еще не испытываются, и до сих пор отсутствуют сообщения о результатах применения соединений, предложенных Вильсоном. Следовательно, пока нужно ограничиться только применением парасимпатических средств. [24]
Конструктивно потенциометрические ферментные редокс-электроды весьма просты. Однако в системах, в которых в реакцию вступает большое количество субстрата, могут возникнуть проблемы, связанные с загрязнением поверхности электрода продуктами ферментативной реакции и отсутствием механизма регенерации фермента. Величина сигнала зависит также от способа предварительной обработки поверхности электрода. Вероятно, потребуются значительные усилия ученых и специалистов, прежде чем ферментные редокс-электроды можно будет рекомендовать для использования в практических целях. [25]
Основная идея о принципах биокатализа возникла еще в начале нашего века благодаря трудам Брауна и Анри и позднее была развита Михаэлисом и Ментен, а также Бриггсом и Холденом. Идея заключается в том, что механизм каталитического действия ферментов состоит в общем случае в образовании между ферментом и субстратом промежуточных соединений, претерпевающих в ходе реакции последовательные превращения вплоть до образования конечных продуктов и регенерации фермента. [26]
В ходе этой реакции молекулы вещества S взаимодействуют с ферментом Е, образуя фермент-субстратный комплекс ES. Затем этот комплекс превращается в конечный продукт Р с регенерацией фермента. [27]
В-третьих, боргидрид натрия, представляющий собой мягкий восстанавливающий агент, реагирующий с CN ( но не С-N), кетонной или амидной карбонильными группами, восстанавливает комплекс фермент - субстрат, полученный из меченного 14С ацетоацетата. В результате образуется продукт, не обладающий ферментативной активностью, в котором при диализе сохраняется практически все количество 14С, и регенерации фермента не происходит. Действие боргидри-да натрия на комплекс фермент - субстрат - цианистый водород с последующим диализом приводит к регенерации фермента, полностью сохранившего свою активность. [28]
Решение этой задачи зависит от возможностей измерения констант скорости этих стадий. По-видимому, наиболее простой могла бы быть оценка влияния температуры на константу скорости распада комплекса Михаэлиса, сопровождающегося образованием продуктов реакции и регенерацией фермента. [29]
В механизме первого типа, или механизме однотактного замещения, субстраты связываются на ферменте в необходимой близости друг от друга, что обеспечивает возможность реакции между ними ( фиг. Таким образом, происходит одна реакция - однотактное замещение. Механизм двухтактного замещения, или образования замещенной формы фермента, предусматривает, напротив, сначала взаимодействие фермента с одним из субстратов с образованием замещенной формы фермента и одного из продуктов реакции. Далее замещенная форма фермента принимает участие во второй реакции замещения с другим субстратом, что приводит к регенерации фермента и образованию второго конечного продукта реакции. [30]
Страницы: 1 2 3