Регистрация - флуоресценция
Cтраница 1
Регистрация флуоресценции в биологии и медицине используется для качественного и количественного анализа веществ ( люминесцентный анализ), а также для изучения - структуры и функции биологических систем различной сложности - от мембран до целых организмов. Иногда эти применения называют флуоресцентным анализом. Большую информацию можно получить, сопоставляя спектр люминесценции и спектр возбуждения люминесценции, а также зная квантовый выход люминесценции. [1]
При регистрации флуоресценции солнечно-сле - [ ым ФЭУ лучшие результаты получаются без диспергирующего фибора. Пределы обнаружения, достигнутые в этих условиях, О 80 Те и 2 нг. [2]
Для регистрации флуоресценции применялись два ФЭУ, работавшие в режиме счета фотонов и включенные по схеме совпадений. Авторам удалось наблюдать среднее число атомов, находящихся в регистрируемом объеме, равное 0 0001 атома. Пока этот предел обнаружения остается рекордным. [3]
Метод основан на регистрации флуоресценции кристаллофосфора на основе вольфрамата кальция, активированного лантанидами. [4]
Это кратковременное люминесцентное свечение называют флуоресценцией, а сам метод, основанный на регистрации флуоресценции, флуориметрией. Флуоресценция при возбуждении света УФ-излучением и используется чаще всего в анализе; она характерна и специфична для каждого вещества, способного люминесцировать. [5]
Для получения максимальной интенсивности флуоресценции в случае применения спектрофлуорометров подбираются параметры обоих монохроматоров для возбуждения и регистрации флуоресценции. Монохроматор для регистрации спектра флуоресценции устанавливают на длину волны, соответствующую максимальной интенсивности спектра флуоресценции. Монохроматором, выделяющим излучение для возбуждения флуоресценции, сканируют возбуждающий спектр. На спектре возбуждения ( кривая а, рис. 5) видны участки поглощения света пробой. Теоретически они должны совпадать со спектром поглощения флуоресцирующего материала. На этом рисунке видны максимумы флуоресценции, соответствующие определенным длинам волн. [6]
Последнее более целесообразно, так как в первом случае на приемник воздействует мешающее излучение пламени за все время регистрации сигнала, а во втором - только в периоды регистрации флуоресценции. [7]
Интересное исследование выполнено Броклехурстом [144], который зарегистрировал магнитный изотопный эффект непосредственно в элементарном акте геминальной рекомбинации пары ион-радикалов. Для регистрации флуоресценции, обусловленной процессом Т Т - у М М ( М и М - основное и синглетное возбужденные состояния ароматической молекулы), использовалась методика измерения времени высвечивания сцинтилляторов методом задержанных совпадений. В этой методике измеряется распределение интервалов времени между моментом возбуждения сцинтиллятора и моментом образования одиночных фотоэлектронов на катоде фотоумножителя, регистрирующего сцинтилляции. Иначе говоря, определяется частота образования фотоэлектронов в узком интервале промежутков времени в зависимости от величины данного промежутка. [8]
Другим примером уменьшения влияния шума рассеянного света является применение нерезонансной флуоресценции, если в спектре источника возбуждения отсутствует аналитическая линия. Так, при регистрации флуоресценции линии Cd 326 1 нм отношение сигнала флуоресценции к шуму рассеянного света возрастает в 10 раз, если возбуждение паров кадмия проводить по линии As 228 812 нм мышьяковистой лампы, в спектре которой нет линии Cd 326 1 нм. При возбуждении флуоресценции при тех же условиях линии Cd 228 802 нм кадмиевой лампы, в спектре которой присутствует линия 326 1 нм, отношение сиг-нал: шум остается неизменным. [9]
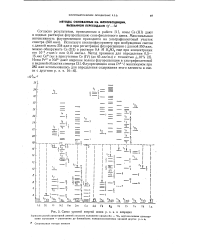 |
Схема уровней энергий ионов р. з. э. в хлоридах. [10] |
Согласно результатам, приведенным в работе [1], ионы Се ( III) дают в водных растворах флуоресценцию сине-фиолетового цвета. Используя спектрофлуориметр при возбуждении светом с длиной волны 254 ммк и при регистрации флуоресценции с длиной 350 ммк, можно обнаружить Се ( III) в растворе 0 4 М H2SO4 еще при концентрации его 10 - 6 г-ион / л или 0 15 мкг / мл. [11]
При реабсорбции концентрация возбужденных молекул изменяется во времени и по глубине образца, при этом возбуждение постепенно распространяется вглубь. Реабсорбция приводит к увеличению времени затухания флуоресценции, отклонению от экспоненци-альности и зависимости характера затухания от длины волны регистрации флуоресценции. Существующая теория реабсорбции, позволяющая охарактеризовать флуоресценцию значениями интегрального времени затухания и оценить неэкспоненциальность по их различию, весьма сложна. [12]
Спектры, приведенные на рис. 176, соответствуют очень низким уровням интенсивности флуоресценции, и, чтобы избежать помех от возбуждающего рассеянного света, для выделения возбуждающего света и регистрации флуоресценции были использованы двойные моно-хроматоры. Хотя примесь, ответственная за спектр с тремя максимумами, была окрашена в желтый цвет, в случаях, которые представлены кривыми на рис. 176 Л, по цвету ее обнаружить не удалось. [13]
Малая угловая расходимость лазерного луча в сочетании с другими положительными свойствами, отмеченными выше, позволяет использовать его для анализа потоков молекул или атомов. Наиболее интересные применения лазеров для этих целей сводятся к следующему: если лазерный луч направить поперек движения потока молекул, то это приведет к уменьшению объема взаимодействия и неоднородности допплеровского контура. Регистрация спонтанной флуоресценции от возбужденных таким образом молекул позволяет определить их поглощательные характеристики. [14]
Во флуориметрах с источником возбуждения, имеющим непрерывный спектр испускания, в качестве осветителя используют низковольтную лампу накаливания. Монохроматизирую-щими устройствами служат скрещенные светофильтры с границей скрещения, соответствующей спектрам возбуждения ( поглощения) и излучения определяемого вещества. Первичный светофильтр ( стеклянный или жидкостный) имеет широкую-область спектрального пропускания, соответствующую полосе поглощения флуориметрируемого раствора; вторичный светофильтр поглощает пропущенный первичным светофильтром лучистый поток ( рассеянный частями прибора и раствором) и по возможности полно пропускает свет, излучаемый определяемым веществом. Такие приборы особенно пригодны для флуориметрирования веществ, слабо поглощающих ультрафиолетовые излучения, но имеющих максимум возбуждения в желтой, оранжевой и красной областях спектра и флуоресцирующих соответственно в его более длинноволновой части. Для регистрации флуоресценции таких веществ следует применять фотоумножители с катодом, область чувствительности которого сдвинута далее к красному концу спектра, чем в приборах с ультрафиолетовыми осветителями. [15]
Страницы: 1 2