Значение - скорость - коррозия
Cтраница 4
Хотя имеющиеся многочисленные данные по сероводородной коррозии металлов в пластовой жидкости и нефтяном газе дают общую ( и реальную) ориентацию в отношении скорости коррозии в этих средах, но эти данные недостаточно информативны в отношении кинетики образования и массы возникающих на металле продуктов его сероводородной коррозии, особенно при длительных экспозициях металла в коррозивной среде. Поэтому нами были проведены в лабораторных условиях длительные коррозионные испытания, целью которых было получение не только значений скорости коррозии во времени, но массы и толщины продуктов коррозии в жидкой и газовой среде. [46]
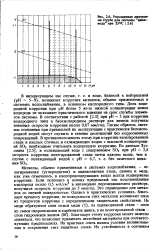 |
Упрощенная дютрам-ма Пурбе для системы нннк-вода при 25 С. [47] |
Доля водородной коррозии при рН более 5 из-за низкой концентрации ионов водорода не оказывает практического влияния на срок службы элементов системы. В соответствии с работой [2.3] при рН 5 при коррозии водородного типа в бескислородном растворе для железа получены значения скорости коррозии около 0 07 мм / год. Таким образом, системы отопления при правильной их эксплуатации с практически бескислородной водой могут служить в течение десятилетий без коррозионных повреждений. В противоположность этому при коррозии нелегированной стали в кислых сточных и охлаждающих водах с высокой концентрацией SOj необходимо учитывать водородную коррозию. [48]
Значения скорости коррозии определяли согласно ГОСТ 9.506 - 87 через 96, 200, 400 и 720 часов выдержки образцов в агрессивной среде. [49]
Скорости коррозии углеродистых и низколегированных сталей, а также чугунов в морской воде отличаются незначительно. Скорость коррозии углеродистой и низколегированной стали в морской воде при полном погружении и длительных испытаниях колеблется в пределах 0 08 - 0 12 мм / год, и максимальный глубинный показатель для стали без окалины составляет 0.3 - 0 4 мм / год. Уже после годичной выдержки достигается достаточно постоянное во времени значение скорости коррозии. Введение легирующих элементов ло 5 % в сталь мало влияет на скорость коррозии. Исключение представляет хром, начиная от 5 % хрома сильно растет местная коррозия стали. Легирование стали одной медью в условиях морской коррозии в отличие от атмосферной коррозии не дает положительных результатов. [50]
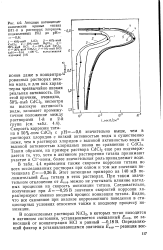 |
Анодные потенциоди-намические кривые титана ВТ1 - 0 в растворах хлоридов, , подкисленных НС1 до рН - 0 6. [51] |
Следовательно, полученные при Е - - 0 26В значения скоростей коррозии характеризуют именно анодный процесс ионизации титана. Видно, что все сказанное при анализе коррозионного поведения в стационарных условиях относится также к анодному процессу ионизации. [52]
По иному механизму протекает коррозионный процесс в установках нагрева морской, воды типа УНТ и БКНУ-ЬООО. Нагрев воды открытым пламенем и насыщение ее продуктами сгорания приводит к резкому увеличению скорости коррозии в морской воде после УПГ и ЕКНУ. Повышенное содержание углекислоты и показание избыточных количеств кислорода при нестабильной работе установки обуславливает значения скорости коррозии до 3 0 мм / год. Интенсивной коррозии подвергаются и отдельные узлы установок нагрева, особенно в высокотемпературной зоне. [53]
На рис. 20 представлены парциальные анодные кривые в координатах потенциал-скорость коррозии в мм / сут. Штриховой линией показан смешанный потенциал полиметаллической конструкции. Величины абсцисс, соответствующих точкам пересечения значения смешанного потенциала и парциальных кривых, показывают логарифмическое значение скорости коррозии в мм / сут. [54]
Как правило, коррозия нержавеющих сталей при температурах 200 - 700 С идет с прибылью массы. Исключение составляет сплав на никелевой основе ХН78Т ( ЭИ435); при давлении 2МПа, температурах 350, 500 С и давлении 5 МПа, температуре 200 С, коррозия этого сплава идет с убылью массы. При постоянных температуре и давлении для широкого ассортимента нержавеющих сталей: хромистых, хромоникелевых, хромоникельмолибде-новых и других, а также ряда сплавов на основе никеля значения скорости коррозии близки между собой, их различия находятся в пределах точности эксперимента. [55]
Понижение скорости коррозии обусловлено понижением температуры, сопровождающейся, по закону Аррениуса, экспоненциальным уменьшением скорости химической реакции. Экстремальное значение скорости коррозии соответствует точке равновесия, в которой количество осажденной кислоты равно количеству росы, вступающей в реакцию с металлом по закону Аррениуса. При дальнейшем снижении температуры стенки и увеличении количества выпадающей росы концентрация кислоты в пленке понижается до 65 - 56 % и скорость коррозии быстро возрастает. В этой области температур значение скорости коррозии может быть выше, чем в точке максимума. [57]
Измерения скорости коррозии в контрольных и испытательных ячейках проводят с помощью коррозиметра. При сопоставлении коррозионной активности необработанной и обработанной магнитным полем жидкости условия обтекания электродов должны быть подобными, а потому рекомендуется вести измерения на одинаковых установках при одинаковых режимах перемешивания жидкости. Замеры начинают через 5 мин после начала перемешивания жидкостей. Среднюю из этих величин принимают за значение скорости коррозии. [58]
 |
Скорость ( 2, 3 и токи коррозии ( 1, 4 сталей в равновесных растворах серной кислоты. - - - - - - - - - - - сталь 1Х18Н9Т. - - - - - - - - - - - - - - - - - сталь 10. [59] |
Для 80 % - ной серной кислоты равновесная температура должна составлять 133 С, однако опыты проводились при температуре 100 С, являющейся как предельной для электрода. Там же кривыми / и 4 представлено изменение значений токов коррозии при нулевой величине электродного потенциала анодных ветвей поляризационных кривых. Сопоставление кривых 2 и 1, 3 и 4 показывает, что характер их изменения весьма близок. Как следует из кривых 1 и 4, значение токов коррозии по закономерности изменения для рассмотренных материалов хорошо согласуется со значениями скорости коррозии их в растворах серной кислоты. [60]
Страницы: 1 2 3 4