Значение - скорость - реакция
Cтраница 4
Если предположить, что она протекает при соударении молекул N2 и 02, то получается значение скорости реакции в тысячу раз меньше того, которое наблюдается в опытах. [46]
Таким образом, можно графически по кривым ij - t ( рис. 2) определить значение скорости реакции растворения в любой момент времени установления равновесия. [47]
В этой же работе показано, что воспламенение в чистом сосуде происходит сразу же после достижения некоторого значения скорости реакции; это указывает на тепловой характер воспламенения. В сосуде же, промытом КС1, воспламенение происходит при гораздо меньших значениях скорости реакции, причем скорость реакции до взрыва в течение всего периода индукции имеет приблизительно постоянную величину. [48]
В этих уравнениях неизвестными являются концентрации трех промежуточных продуктов [ Х2 ], [ Х3 ], [ Xt ] и значение скорости реакции R. [49]
Исследование влияния природы алкильной группы в галоидалкиле показывает, что при возрастании электронодонорных свойств R в галоидалкиле RX скорость увеличивается; так, например, значение скоростей реакций больше для третичных алкильных групп, чем для вторичных, и еще меньше в случае первичных групп. Наконец, скорости реакций оказываются большими в присутствии катализаторов, о которых известно, что они обладают лучше выраженными электроноакцепторными свойствами; так, хлористый алюминий является более активным катализатором, чем хлориды олова или цинка, в то время как хлориды кремния и натрия неактивны. [50]
Дополнительно заметим, что распределение скоростей по зерну не играет роли при анализе теплообмена зерна ( или слоя зерен) с окружающей средой; существенно значение скорости реакции и, соответственно, тепловыделения, для зерна в целом. [51]
Для расчета пределов самовоспламенения необходимо с помощью закона действующих масс найти аг Чтобы учесть роль диаметра сосуда, закон действующих масс применяют не с подсчетом значения скорости реакций в единице объема, как это обычно делается, а с подсчетом скорости данного вида реакций во всей реагирующей системе. [52]
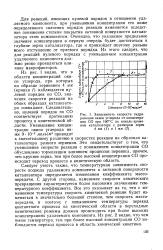 |
Зависимость скорости гидрирования окиси углерода от концентрации СО при 160 С на никель-хромовом катализаторе с размером зерен 4 мм ( 1 и 1 мм ( 2. [53] |
Из рис. 1 видно, что в области концентраций окиси углерода, при которых на образце зернением 4 мм ( кривая 1) наблюдается нулевой порядок по СО, значения скорости реакции на обоих образцах катализатора совпадают. Следовательно, нулевой порядок по СО соответствует протеканию процесса в кинетической области. [54]
Для построения кривой, выражающей зависимость скорости реакции от концентрации одного из реагирующих компонентов, определяют первые производные из уравнения кривой кинетики процесса для целого ряда значений концентраций, которые и являются значениями скорости реакции. [55]
Из (1.9) следует, что определение скорости реакции как изменения концентрации любого из исходных веществ или продуктов реакции, отнесенного к соответствующему стехиометрическому коэффициенту, независимо от выбранного вещества, приводит к одному и тому же значению скорости реакции. [56]
Страницы: 1 2 3 4