Значение - сродство
Cтраница 3
Такой зависимости нет, так как на соотношение значений сродства к электрону и потенциалов ионизации сильно влияет структура электронной оболочки атома. Это можно наблюдать у атомов инертных элементов, потенциал ионизации которых велик, так как их энергетические уровни устойчивы, однако по той же причине их сродство к электрону очень мало. [31]
Почти для всех атомов, за исключением галогенов, значение сродства примерно на порядок меньше значения потенциала ионизации. [32]
Одним из наиболее сильных акцепторов электронов является тетрацианэтилен74 со значением сродства к электрону 1 6 эв, который очень легко образует окрашенные комплексы со многими ароматическими углеводородами. [33]
Одним из наиболее сильных акцепторов электронов является тетрацианэтилен со значением сродства к электрону 1 6 эв [52], который очень легко образует окрашенные комплексы со многими ароматическими углеводородами. [34]
Чтобы вникнуть в проблему несколько глубже, обратимся к ионизационным потенциалам и значениям сродства к электрону, а также к энергиям диссоциации в последовательности молекул С2, N2, O2 и сравним их с характеристикой атомов С1, Аг, К. [35]
Для того чтобы такая реакция протекала слева направо ( была положительной), значение сродства должно быть отличным от нуля и выходить за пределы, соответствующие метастабильной области. [36]
Сравните галогены друг с другом, пользуясь табл. 5, где в пункте 6 приведены значения сродства галогенов к электронам, а в пункте 8 значения энергии связи атомов в молекулах галогенов, характеризующих прочность связи. Как видно, прочность связи существенно меньше сродства к электрону для всех галогенов. Прочность связи для фтора равна всего 37 ккал / моль, а для хлора 57 87 ккал / моль. Очевидно, атомам галогенов энергетически выгодно находиться в состоянии, возможно близком к состоянию иона, которого он полностью достигает, становясь свободным анионом в водном растворе. Это является основной причиной того, что в природе галогены встречаются почти исключительно в виде отрицательных ионов. [37]
Если продукты разложения не возбуждены, то измерение потенциала появления и кинетической энергии осколков позволяет получить значение сродства к электрону нейтральной частицы В, соответствующей отрицательному иону. [38]
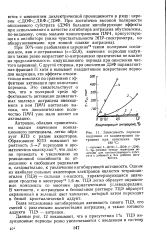 |
Зависимость периода индукции от концентрации антрацена при окислении при 180 С. [39] |
Одним из наиболее сильных акцепторов электронов является тетрациан-этилен ( ТЦЭ) - сильная тг-кислота, характеризующаяся значением сродства к электрону73 1 6 эв. ТЦЭ легко образует окрашенные комплексы со многими ароматическими углеводородами. В частности, с антраценом в бензольном растворе ТЦЭ образует окрашенный в зеленый цвет комплекс, который затем переходит в белый кристаллический аддукт. [40]
 |
Радиусы Ван-дер - Ваальса rw атома хлора в молекуле С12. [41] |
Главный недостаток метода Мал-ликена заключается в том, что далеко не всегда можно с высокой точностью определить значение сродства к электрону. [42]
Функция диссипации ( см. (6.6)) не определена в том смысле, что не указано, о каких значениях сродства si идет речь - о внешних или внутримембранных. Согласно [34], можно провести соответствующее уточнение. [43]
Небольшое изменение коэффициентов диффузии дисперсных красителей при проникновении в полиэфирное волокно при 25 и 40 С, а также близость значений сродства красителя к волокну и растворителю свидетельствует о том, что движущей силой такого процесса крашения является растворение красителя в метиленхлориде, находящемся в волокне. [44]
Было определено также сродство к электрону некоторых переходных металлов [2]; золото, которое, как известно, образует соединение Cs AiT, имеет значение сродства к электрону около 2 2 эв, в то время как Ag, Cu, Pd и Pt имеют значения сродства не менее чем 1 эв. [45]
Страницы: 1 2 3 4