Редлих
Cтраница 3
Редлих и Данлоп [74], а также Аккерман [75] добавили в него дополнительные члены, использовав фактор ацентричности в качестве третьего коррелирующего параметра. По Аккерману ZRK - некорректированный коэффициент сжимаемости, рассчитанный по уравнению Редли-ха - Квонга. [31]
Этому простому виду корреляции соответствуют лишь смеси соединений со сходными химическими свойствами. Например, Редлих ( 1976) приводит шесть двухкомпонентных смесей этилбензола и изомеров ксилола; в этом случае, однако, константы варьируют лишь в пределах от 0 0035 до 0 0003, а это свидетельствует о том, что поведение по существу идеально. Смеси, показанные на рис. 4.5, а также демонстрируют поведение, близкое к симметричному, но для них отклонения от идеальности довольно значительны. [32]
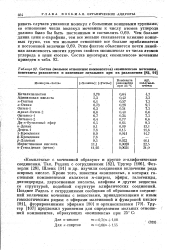 |
Состав ( мольное отношение компонентов комплексов мочевины, константы равновесия и изменение энтальпии при их разложении. [33] |
Комплексы с мочевиной образуют и другие н-алифатические соединения. Так, Редлих с сотрудниками [82], Трутер [106], Фет-терли [28], Шленк [91] и др. изучили соединения включения ряда жирных кислот. Кроме того, известны комплексы, в которых гостевыми компонентами являются н-спирты, эфиры, галогениды, диглицериды, двухосновные кислоты, олефины и другие вещества со структурой, подобной структуре алифатических соединений. [34]
Этому простому виду корреляции соответствуют лишь смеси соединений со сходными химическими свойствами. Например, Редлих ( 1976) приводит шесть двухкомпонентных смесей этилбензола и изомеров ксилола; в этом случае, однако, константы варьируют лишь в пределах от 0 0035 до 0 0003, а это свидетельствует о том, что поведение по существу идеально. Смеси, показанные на рис. 4.5, а также демонстрируют поведение, близкое к симметричному, но для них отклонения от идеальности довольно значительны. [35]
Этот выбор сделан произвольно и главным образом по соображениям большего удобства. Хичкок [ 25а ] и Редлих и Клингер [256] проанализировали возможные преимущества применения электродов сравнения, обратимых по отношению к одновалентному катиону. [36]
Ван-дер - Ваальса ( 1873) или уравнения Клаузиуса ( 1880), хотя и было разработано спустя 70 лет. В своей книге, опубликованной в 1976 г., Редлих [580] пишет, что разрабатывая это уравнение состояния, они не руководствовались какими-либо определенными теоретическими обоснованиями, поэтому его можно рассматривать как произвольную, но удачную эмпирическую модификацию предшествующих уравнений. Вскоре после опубликования уравнения Ван-дер - Ваальса выяснилось, что параметр а заметно зависит от температуры, так что для введения члена Т0 5 имелись определенные посылки. [37]
 |
Степень диссоциации азотной кислоты при температуре, близкой к 25. [38] |
Вопрос о диссоциации умеренно сильных и очень сильных электролитов был рассмотрен в обстоятельном обзоре Редлиха [45] 1, который уделил значительное внимание тем несомненным доказательствам присутствия недиссоциированных молекул, которые могут быть получены на основании изучения рамановских спектров. Наличие вибрационных спектров представляет собой тот критерий, с помощью которого можно надежно отличать молекулы от взаимодействующих между собой ионов. Редлих и Розен-фельд [46] полагают, что истинную концентрацию ионов в данном растворе можно определить путем сравнения спектра этого раствора со спектром раствора полностью диссоциированного электролита, содержащего тот же ион. Как известно, интенсивность рамановских спектров нитратов щелочных металлов пропорциональна их концентрациям [47, 48], что является доказательством полной диссоциации этих солей. Для определения концентрации нитрат-ионов ас в растворе азотной кислоты со стехиометрической концентрацией с приготовляют такой раствор азотнокислого натрия, у которого интенсивность рамановских спектров равна интенсивности соответствующих спектров, наблюдаемых в случае раствора азотной кислоты. Поскольку стандартный раствор нитрата с концентрацией ск полностью диссоциирован. [39]
Однако в работе Рао и в других аналогичных исследованиях [127] в течение десятилетия ( 1930 - 1940 гг.) не был точно определен коэффициент пропорциональности между интенсивностью и концентрацией. Редлих и сотрудники более успешно исследовали азотную [128] и хлорную [129] кислоты, хотя этот метод осложняется использованием фотографических пластинок. Затруднения возникают из-за логарифмических показаний пластинок, и нельзя предположить, что почернение пластинки пропорционально интенсивности. Даже если, например, концентрация нитрат-ионов в азотной кислоте определяется путем подбора раствора нитрата натрия с одинаковой интенсивностью главной рамановской линии нитрат-иона, то возникают большие ошибки в результате уширения линии. [40]
Таким образом, Англа не смог выявить нестехиометрический характер этих веществ и принадлежность их к соединениям включе ния. Истинная природа последних была установлена Смитом [98], который применил метод дифракции рентгеновских лучей. Редлих с сотрудниками [83], Шленк [91] и другие исследователи [67] основательно изучили термодинамические и другие свойства этих веществ. [41]
 |
Степень диссоциации азотной кислоты при температуре, близкой к 25. [42] |
Вопрос о диссоциации умеренно сильных и очень сильных электролитов был рассмотрен в обстоятельном обзоре Редлиха [45] 1, который уделил значительное внимание тем несомненным доказательствам присутствия недиссоциированных молекул, которые могут быть получены на основании изучения рамановских спектров. Наличие вибрационных спектров представляет собой тот критерий, с помощью которого можно надежно отличать молекулы от взаимодействующих между собой ионов. Редлих и Розен-фельд [46] полагают, что истинную концентрацию ионов в данном растворе можно определить путем сравнения спектра этого раствора со спектром раствора полностью диссоциированного электролита, содержащего тот же ион. Как известно, интенсивность рамановских спектров нитратов щелочных металлов пропорциональна их концентрациям [47, 48], что является доказательством полной диссоциации этих солей. Для определения концентрации нитрат-ионов ас в растворе азотной кислоты со стехиометрической концентрацией с приготовляют такой раствор азотнокислого натрия, у которого интенсивность рамановских спектров равна интенсивности соответствующих спектров, наблюдаемых в случае раствора азотной кислоты. Поскольку стандартный раствор нитрата с концентрацией Сд полностью диссоциирован. [43]
Редлих пытался привести пример [13], когда обобщенная сила является экстенсивной величиной. При последовательном соединении двух одинаковых гальванических элементов разность потенциалов, конечно, удваивается. Отсюда Редлих и делает вывод о том, что разность потенциалов ( обобщенная сила) - экстенсивная величина. Вывод этот основан на недоразумении. При делении системы на части, соединении отдельных частей в одну систему, кроме размеров системы, в ней ничего не должно измениться. Редлих же изменяет способ присоедчнения проводов. [44]
 |
Взаимное притяжение дипольных молекул. [45] |
Страницы: 1 2 3 4