Значение - теплота - растворение
Cтраница 2
Как видно из табл. 6, значения теплоты растворения пропилена во всех исследованных растворителях близки между собою и составляют 4000 - 4500 кал / моль. [16]
 |
Диаграмма /, с для раствора. [17] |
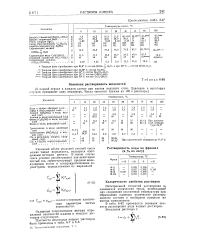
В табл. 5 - 98 приводятся значения теплоты растворения водных растворов. [18]
 |
Взаимная растворимость жидкостей. [19] |
В табл. 6 - 62 приводятся значения теплоты растворения ряда водных растворов. [20]
По прямой графика IgP-1 / Г вычислили значение теплоты растворения азота в метилциклогексане, которое равно 1 0 ккал / моль. [21]
Адсорбционные взаимодействия в статическом методе практически отсутствуют, поэтому значения теплот растворения в этом методе меньше, чем в хроматограф ическом. [22]
 |
Разбавление пересыщенного раствора до насыщенного. [23] |
Во-вторых, в точке т0 для насыщенного раствора отмечают значение последней теплоты растворения, которое для изотермы равно нулю. [24]
 |
Результаты вычислений теплоты сублимации свинца. [25] |
Быховский и Россини [813] на основании измеренных Томсеном [3981] значений теплоты растворения окиси свинца в азотной кислоте и теплоты осаждения хлористого свинца хлористым калием вычислили для теплоты образования окиси свинца величину - 52 91 ккал / моль. [26]
По уравнениям ( 2) и ( 6) рассчитаны значения теплот растворения ацетилена в Л - метил-2 - пирролидоне и диоксане, равные соответственно 6 53 и 4 62 ккал / моль. [27]
 |
Кажущиеся энтальпии НС1 и теплоты растворения и разбавления в системе Н2О - НС1. [28] |
Так как по закону Гесса искомая величина равна разности между значением теплоты растворения исходного и конечного растворов, то в соответствии с ними ( см. рис. 75) при смешении будет выделяться 3 6600 - 1 813 9400 2760 ккал. [29]
Значение изменения энтальпии перехода газа из стандартного состояния в раствор равно значению теплоты растворения газового компонента с обратным знаком. Эта теплота выделяется при переходе компонента из стандартного состояния в равновесный с ним водный раствор. При дальнейшем повышении концентрации компонента в растворе, необходимой для достижения конечного состояния процесса ( гипотетического чистого компонента), энтальпия не меняется, поскольку принимается соблюдение закона Генри. [30]
Страницы: 1 2 3 4