Значение - энергия - возбуждение
Cтраница 2
Они упомянуты здесь в порядке убывания энергии возбуждения. Значение энергии возбуждения электрона в молекуле обычно порядка ее потенциала ионизации Jm, однако многие молекулы имеют иногда несколько низко лежащих электронных термов. Значение энергии возбуждения колебательных степеней свободы обычно порядка ее энергии диссоциации. Лишь энергии диссоциации молекул инертных газов весьма малы 0 01 эВ, поэтому они даже при очень низких температурах являются атомарными газами. Энергия возбуждения вращательных степеней свободы для большинства молекул лежит в интервале 10 - 2 - 10 - 1 эВ, так что в интересующей нас области температур вращение молекул всегда квазиклассично. [16]
В новой теории принимается, что только классические степени свободы определяют движение реакционной системы через потенциальный барьер. Все степени свободы делят на классические и квантовые, в зависимости от значения энергии возбуждения А. [17]
Постулируется, что нуклон может находиться не только в обычном состоянии, характеризуемом спинами / - / V2 и массой М, но также в изобарном состоянии со спинами 4 / - / - 3 / 2 и массой М1М А. Значение энергии возбуждения Д не выводится из каких-либо теоретических соображений, а подбирается так, чтобы по возможности удовлетворить опытным данным. Взаимодействие нуклонов с мезонами характеризуется тремя константами: константой псевдовекторного взаимодействия g / p ( где р - масса мезона), константой псевдоскалярного взаимодействия g sg ( где s - число) и константой gl7 определяющей вероятность таких процессов поглощения или излучения мезонов, при которых нуклон переходит из невозбужденного состояния в изобарное, или обратно. [18]
Они упомянуты здесь в порядке убывания энергии возбуждения. Значение энергии возбуждения электрона в молекуле обычно порядка ее потенциала ионизации Jm, однако многие молекулы имеют иногда несколько низко лежащих электронных термов. Значение энергии возбуждения колебательных степеней свободы обычно порядка ее энергии диссоциации. Лишь энергии диссоциации молекул инертных газов весьма малы 0 01 эВ, поэтому они даже при очень низких температурах являются атомарными газами. Энергия возбуждения вращательных степеней свободы для большинства молекул лежит в интервале 10 - 2 - 10 - 1 эВ, так что в интересующей нас области температур вращение молекул всегда квазиклассично. [19]
В соответствии с правилом Гунда атом никеля в основном состоянии имеет два непарных d - электрона, атом кобальта - три, атом хрома - шесть ( пять 3d и один 4s), атом палладия - ни одного, атом платины - два ( один 5d и один 6s), атом иридия - три. Проявление иных значений ковалентности связано с переходом в возбужденное состояние. Для переходных элементов значения энергии возбуждения относительно невелики. [20]
В соответствии с правилом Гунда атом никеля в основном состоянии имеет два непарных d - электрона, атом кобальта - три, атом хрома - шесть ( пять 3d и один 4s), атом палладия - ни одного, атом платины - два ( один 5d п один 6s), атом иридия - три. Проявление иных значений ковалентности связано с переходом в возбужденное состояние. Для переходных элементов значения энергии возбуждения относительно невелики. Это последнее обстоятельство не дает возможности с уверенностью решать вопрос о том, какие электроны будут принимать участие во взаимодействии атомов данных элементов с другими атомами, при посредстве которых осуществляется ком-плексообразование. [21]
Если энергия возбуждения, привнесенная в ядро при захвате теплового нейтрона, окажется меньше § f, то возникающие деформации не достигнут критического значения и ядро не испытает деления под действием теплового нейтрона. Эти простые представления позволяют понять, почему одни ядра - U235, U233, Pu230 - делятся под действием тепловых нейтронов, а другие - U2 18, U234, Th232 - делятся лишь под действием быстрых нейтронов. В четвертой и пятой колонках таблицы 13 приводятся значения энергии возбуждения и активации для некоторых ядер. [22]
Так же как в низкомолекулярных сопряженных системах, с ростом цепи сопряжения ( например, при переходе от бензола к пентац ену) изменяется энергетическая характеристика вещества и соответственно его электрические и магнитные свойства и реакционная способность. Свойства полимеров с системой сопряжения зависят от молекулярной массы, и вследствие этого полимергомологи могут значительно различаться по свойствам. С возрастанием молекулярной массы полимеров изменяется длина сопряженной системы и ее энергетическая характеристика - значение энергии возбуждения. С изменением последней изменяется реакционная способность и физические свойства молекул. Реакционная способность функциональных групп полимера, если они входят в систему сопряжения, зависит от его молекулярной массы. [23]
Так же как в низкомолекулярных сопряженных системах, с ростом цепи сопряжения ( например, при переходе от бензола к пен-тацену) изменяется энергетическая характеристика вещества и соответственно его электрические и магнитные свойства и реакционная способность. Свойства полимеров с системой сопряжения зависят от молекулярного веса и вследствие этого полимергомологи могут значительно различаться по свойствам. С возрастанием молекулярного веса полимеров изменяется длина сопряженной системы и ее энергетическая характеристика - значение энергии возбуждения. [24]
Так же как в низкомолекулярных сопряженных системах, с ростом цепи сопряжения ( например, при переходе от бензола к пентацену) изменяется энергетическая характеристика вещества и соответственно его электрические и магнитные свойства и реакционная способность. Свойства полимеров с системой сопряжения зависят от молекулярной массы, и вследствие этого полимергомологи могут значительно различаться по свойствам. С возрастанием молекулярной массы полимеров изменяется длина сопряженной системы и ее энергетическая характеристика - значение энергии возбуждения. С изменением последней изменяется реакционная способность и физические свойства молекул. Реакционная способность функциональных групп полимера, если они входят в систему сопряжения, зависит от его молекулярной массы. [25]
В молекулярных кристалла ковалентная связь внутри молекулы значительно сильнее ван-дер-ваальсовой связи между молекулами. Линии - спектра поглощения молекулярного кристалла, обусловленные возбуждением электронов внутри структурных единиц, будут проявляться в спектре кристаллического тела как экситонные линии, иногда несколько смещенные по частоте. В случае щелочно-галюидных кристаллов экситоны с наименьшими энергиями локализованы на отрицательных ионах галогенов, так как значения энергии возбуждения электронов в отрицательных иолах меньше, чем в положительных. [26]
Поэтому использование молекулярных орбиталей при рассмотрении вопросов, связанных с процессами возбуждения и ионизации, дает определенные преимущества. Разница в энергии различных лшогоэлектронных состояний определяется, таким образом, в основном как изменение энергии, вызванное переходом отдельного электрона с одного уровня на другой, как если бы взаимодействие между электронами отсутствовало. Конечно, при этом следует проявлять известную осторожность. В частности, сказанное неверно, если, например, формула (5.5.5) дает одно и то же значение энергии возбуждения для двух различных переходов; в этом случае для описания возбужденного состояния необходимо использовать две конфигурации. Тем не менее именно указанное понимание процессов возбуждения и ионизации обусловило большой успех модели независимых частиц ( характерной чертой которой является использование в качестве волновой функции отдельного спин-орбитального произведения); оно дает простое объяснение большому числу экспериментальных данных. [27]
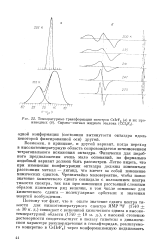 |
Температурные трансформации спектров CsIrFB ( а и их производных ( б. Справа-сигнал жидкого эталона ( CC12F2. [28] |
Возможен, в принципе, и другой вариант, когда переход в высокотемпературную область сопровождается исчезновением тетрагонального искажения октаэдра. Физически для подобного предположения очень мало оснований, но формально подобный вариант должен быть рассмотрен. Легко видеть, что при изменении конфигурации октаэдра должны изменяться расстояния металл - лиганд, что влечет за собой изменение химических сдвигов. Чрезвычайно маловероятно, чтобы новое значение химического сдвига совпадало с положением центра тяжести спектра, так как при изменении расстояний сложным образом изменяется ряд величин, в том числе основные для химического сдвига - молекулярные орбитали и значения энергий возбуждения. [29]
Страницы: 1 2