Вес - атом
Cтраница 2
Ю-24 - вес атома водо рода в г; А - атомный вес. Для германия при 1000 С в результате расчета по формуле ( 58) получается N 4 56 - Ю22 см-3. Сравнивая NI и N, можно заключить, что структура ближнего порядка германия, а по аналогии с ним и кремния, представляет собой размытый объемноцентрирован-ный куб. [16]
Для определения веса атома в химии введена условная кислородная единиц а. Кислородной единицей называется 1 / ie веса атома кислорода. [17]
Обосновывая выбор веса атома кислорода в качестве единицы сравнения атомных весов, Берцелиус писал: Сравнение веса атома с весом водорода не дает никаких преимуществ, а, пожалуй, скорее, много неудобств, ибо водород является слишком легким телом и встречается реже в неорганических соединениях. Напротив, кислород объединяет в себе все преимущества и является, так сказать, центром, вокруг которого вращается вся химия. Он входит в состав всех органических и большинства неорганических тел [ 24, стр. [18]
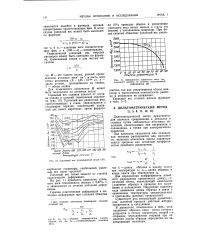 |
Удельный вес углеродистой стали.| Зависимость удельного веса тех. [19] |
Vie часть веса атома кислорода ( А 1 65 10 - 24 г); п - число атомов, приходящихся на ячейку; V - объем ячейки. [20]
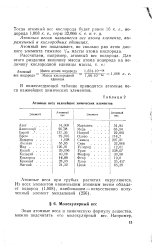 |
Атомные веса важнейших химических элементов. [21] |
Атомным весом называется вес атома элемента, выраженный в кислородных единицах. [22]
Может быть, вес атома урана должно увеличить-в два раза потому уже, между прочим, что столь тяжелые ( плотность-18 4) металлы, как уран, встречаются только между имеющими большой атомный вес. Примером служит платина, осмий и иридий. Сними сходны палладий, родий и рутений, их плотность около 11, а вес атома около 105, [383] Уменьшилась плотность, убавился и вес атома. Уран стоит, по-видимому, в таком же отношении к элементам железного ряда, как Pt и Р1; его пай ( 120) и его плотность в два с лишком раза болеег чем железа и его аналогов. Но если пай урана близок в то же время к паю палладия, родия и рутения, то плотность в два раза почти более. При малом атомном весе в SO2 нет и следов основных свойств, при значительном весе теллура в его окисле ТеО2 уже обозначена слабая способность соединяться с кислотами и свойства слабой кислоты. [23]
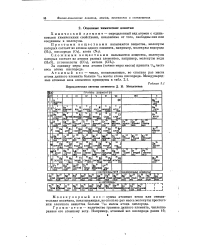 |
Периодическая система элементов Д. И. Менделеева. [24] |
За единицу меры веса атомов ( точнее меры массы) принята Vie часть веса атома кислорода. [25]
Принимая для величины веса атома Н1, а для теплоемкости воду 1; для газов везде взята теплоемкость при постоянном давлении, отнесенная к единице веса. [26]
Частное от деления веса атома на удельный вес элемента выражает удельный объем, который пропорционален объему атомов. Кубический корень из этого частного выражает расстояние атомов друг от друга и для этих элементов будет наименьшим. Следовательно, атомы в частицах этих элементов наиболее сближены; частное равно почти 7 5 для верхнего ряда, для нижнего - 9 5; между тем как для калия, например, это частное равно 35, для хлора - 27, следовательно, в разбираемых элементах атомы наиболее сближены, трудноподвижны, а потому эти элементы трудно будут вступать в химические соединения. [27]
Истинные и относительные веса атомов и молекул. [28]
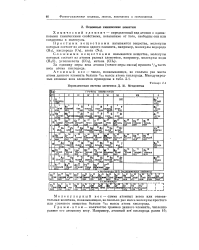 |
Периодическая система элементов Д. И. Менделеева. [29] |
За единицу меры веса атомов ( точнее меры массы) принята Vie часть веса атома кислорода. [30]
Страницы: 1 2 3 4