Значение - энергия - активация - реакция
Cтраница 2
Пиз и Вальц [10] экспериментально нашли значение энергии активации реакции хлорирования метана, которая оказалась равной 31 6 ккал / моль. [16]
Общий интерес представляет установленный им факт увеличения значений энергии активации реакции гидролиза с ростом основных свойств амина. [17]
Полученные данные подтверждают, что при высоких температурах по значению энергии активации реакции окисления коксовых отложений и кокса нельзя судить об истинной энергии активации. Поэтому энергию активации следует определять для конкретного узкого интервала температур, так как она становится функцией температуры. [18]
В указанных работах приводится только одно значение энергии активации, близкое значению энергии активации реакции С СС2, и на основании этого делается вывод, что данная реакция является определяющей в течение всего периода восстановления от высшего окисла до металла. [19]
Для предварительного суждения о наиболее вероятном механизме реакции нужно обратить внимание на значение энергии активации реакций соединения водорода с галоидами. [20]
Примерно одинаковые значения энергии активации для различных процессов ( 45 ккал / молъ), близкие значению энергии активации реакции восстановления ССЬ графитом [94, 95], позволили авторам сделать вывод, что в вакууме и при давлениях, близких атмосферному, скорость процесса определяется этой реакцией. [21]
Полученное выражение соответствует экспериментальному при Е2а - 6 ккал / моль и Р2а / р го Ю-5. Значение энергии активации реакции присоединения jEja 6 ккал / моль вполне разумно. Значение рт вследствие проявления клеточного эффекта, по всей вероятности, равно 1, следовательно, рга. Для реакции присоединения сложного высокомолекулярного радикала к системе я-связей алкилированных ароматических систем такое значение возможно. [22]
Изучена кинетика реакции нуклеофильиого замещения атомов хлора в 4-хлорзамещенных дифеннлсульфонах на фенокси - и тиофе-нильные группы. Найдены значения энергий активации реакций, последовательного замещения атомов хлора в 4 4 / - днхлордифенилсульфо-не равные 80 8 и 108 3 кДж / моль. Исследована реакционная способность 4-замещенных 4 / - хлордифенилсульфонов и замещенных фенолов и тиофенолов в указанной реакции с использованием уравнения Гам-мета. [23]
Изучена кинетика реакции пуклеофнлыюго замещения атомов хлора в 4-хлор-замещенпых днфепилеульфопах па фепоксн - и тиофепнлыше группы. Найдены значения энергий активации реакций последовательного замещения атомом хлора в 4 4 / - днхлордпфепилеульфопе равные 80 8 и 108 3 кДж / моль. Исследована реакционная способность 4-замсщенных 4 -хлордпфепилсульфопов и замещенных фенолов и тиофенолов в указанной реакции с использованием уравнения Гаммета. [24]
 |
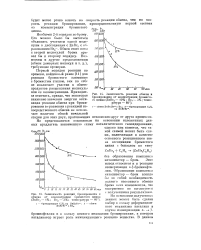
Изменение степени восстановления окиси железа с течением времени при вое-становлении окисью углерода ( 1 и водородом ( 2. [25] |
При степени восстановления окиски железа до 40 % значение энергии активации остается примерно постоянным и составляет 16 5 - 17 1 ккал / моль. Эти значения энергии активации реакции восстановления РеаОз водородом соответствуют величинам, полученным Чуфаровым и Ростовцевым. [26]
Чжоу Шао-минь исследовал кинетику чисто химического окисления большого ряда спиртов и параллельно изучил кинетику электрохимического окисления тех же спиртов в альдегиды. Он показал, что между значениями энергии активации реакций чисто химического окисления спиртов и электрохимического окисления тех же спиртов существует согласованность. [27]
Скорость каталитических реакций часто существенно зависит от температуры. Для оценки влияния температуры на скорость реакции служит значение энергии активации реакции Е и температурный коэффициент а, который показывает, во сколько раз увеличивается скорость реакции при увеличении температуры на 10 С. [28]
Первый порядок реакции по времени найденный ранее [11] для реакции бромистого алюминия с бромистым этилом, сам по себе не исключает участия в обмене продуктов расщепления молекулы или ее полимеризации. Приходится отметить, правда, что некоторое снижение значения энергии активации реакции обмена при броми-ровании в сравнении с реакцией непосредственного обмена не исключает наличия общей начальной стадии для этих двух, протекающих независимо друг от друга процессов. [30]
Страницы: 1 2 3