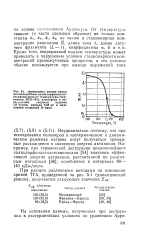
Значение - эффективная энергия - активация
Cтраница 2
Графически или методом наименьших квадратов находят значения эффективной энергии активации процесса Q и постоянной А уравнения ( 114) и проверяют правильность полученного эмпирического уравнения температурной зависимости скорости коррозии металла в растворе кислоты: рассчитывают по полученной эмпирической формуле значение Km для какой-либо температуры и сравнивают его с опытным значением. [16]
В табл. 11 собраны данные со значениями эффективных энергий активации образования гидроперекисей при радиационном окислении к-нонана в терморадиационной области. [17]
Таким образом, мы видим, что значения эффективной энергии активации в области высоких давлений, где ЕЭФФ - Е0, и в области малых давлений не совпадают. [18]
Из температурной зависимости константы скорости окисления вычислено значение эффективной энергии активации процесса окисления, равное 35 5 ккал. [19]
В табл. 6 приведены вычисленные из этих графиков значения эффективной энергии активации процесса окисления сплавов. [20]
Положительное влияние ультразвука появляется при этом тем сильнее, чем ниже значения эффективной энергии активации. [21]
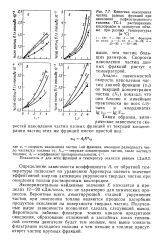 |
Кинетика накопления частиц разных фракций при окислении нефильтрованного топлива ТС-1 растворенным кислородом в замкнутом объеме при разных температурах ( в С. [22] |
Определение зависимости коэффициента Л, от обратной температуры позволяет по уравнению Аррениуса оценить значение эффективной энергии активации укрупнения твердых частиц при окислении топлив растворенным кислородом. [23]
Как мы видели выше, при n 2f - 1 тождественными оказываются также получаемые в обеих теориях значения эффективной энергии активации. Так как в теории Сле-тера, как и в теории Касселя, п и f обозначают одну и ту же величину - число колебательных степеней свободы активной молекулы, причина несоответствия чисел п и / физически неясна. По мнению Слетер а, возможной причиной этого несоответствия является то, что в то время как в теории Касселя активированная молекула определяется как молекула, на одной или нескольких степенях свободы которой концентрируется критическая энергия Е0, в теории Слетера критерием активированной молекулы служит выражаемое условием (17.28) некоторое критическое значение амплитуды колебаний. [24]
Полученные с помощью ( 8 - 64) из опытных данных по зависимости lnUT f ( l / 7V) значения эффективной энергии активации Еа для реакции в турбулентных пламенах близки к энергии активации основной реакции разветвления. Эта величина также близка к значению Е реакций в ламинарных пламенах тех же смесей. Следовательно, ламинарные и турбулентные пламена сходны в том отношении, что в них реакции развиваются в ходе перемешивания свежей смеси с продуктами сгорания. Вместе с тем различная зависимость скорости горения от скорости реакции в ламинарном и турбулентном пламенах свидетельствует о коренном различии механизма распространения пламени в условиях массо-обмена через молекулярную и турбулентную диффузию. [25]
Результаты этих экспериментальных исследований позволили выяснить условия, обеспечивающие образование при хлорировании н-бутана практически исключительно монохлорбутанов, и впервые определить значение эффективной энергии активации термического хлорирования н-бутана и изобутана. Наряду с этим была установлена роль поверхности реакционного сосуда в гетерогенном зарождении цепей. Этот вопрос был подробно рассмотрен выше ( см. стр. [26]
На основании уравнения Аррениуса ( 4) по данным работ [ 44 и 82 ], полученным в результате окисления гудронов при разных температурах, были рассчитаны значения стандартной эффективной энергии активации. Сопоставимость этих значений, вычисленных в результате независимых расчетов по данным окисления гудронов различных нефтей, свидетельствует о правильности выбранного общего аналитического вида зависимости скоростей образования асфальтенов. [27]
Зависимости, сходные с представленными на рис. 6 и 7, были получены для всех испытанных топлив при различных давлениях. Приводим значения эффективных энергий активации Еэфф реакций, предшествующих появлению холодных пламен, вычисленные по соответствующим наклонам прямолинейных участков кривых IgTxmi / ( 1 / Т0) значения эффективных порядков реакции гсэфф, вычисленные по полученному сокращению тхпл при Т0 450 С при изменении Р0 от 2 5 до 5 ата, начальные температуры смеси Т0, отвечающие максимумам ДРХпл при Р0 2 ama, a также октановые числа О. [28]
Согласно работе [63] скорость хлорирования высших хлорэтанов в жидкой фазе в интервале 43 - 85 С пропорциональна их концентрации. Для всех хлорэтанов получено значение эффективной энергии активации, равное 62 3 кДж / моль, что маловероятно, - по данным газофазного хлорирования эта величина значительно ниже и сильно отличается при изменении объекта хлорирования. [29]
Страницы: 1 2 3