Результат - применение - уравнение
Cтраница 2
В данной работе проведено сопоставление результатов расчетов с применением девяти уравнений состояния, начиная от уравнения Ван-дер - Ваальса и кончая уравнением Бенедикта - Уэбба - Рубина, с данными, полученными экспериментальным путем для таких веществ, как аргон и бугаи. В некоторых случаях результаты применения уравнений сравнивают между собой. [16]
Предположим, что одновременно между собой реагируют пять компонентов: Н2, О2, HzO, CO и СО2, причем существующие условия таковы, что атомарные углерод, кислород и водород в равновесной смеси практически отсутствуют. Рассмотрим, что можно получить в результате применения уравнения (19.11) для определения равновесного состава. Прежде всего нужно определить минимальное число независимых стехиометрических уравнений, необходимое для описания всех реакций с участием данных пяти компонентов. С этой целью запишем три уравнения, представляющие соответственно сохранение количества атомов углерода, водорода и кислорода в процессе перехода между двумя бесконечно близкими устойчивыми состояниями. [17]
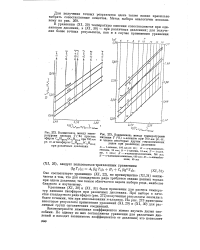
Уравнения ( XI, 30) и ( XI, 31) были применены для расчета температур кипения тиоэфиров при различных давлениях. На рис. 273 приведены некоторые результаты применения уравнений ( XI, 29) и ( XI, 30) для различных групп органических соединений. [19]
Компактная конформация сывороточного альбумина несколько более устойчива в щелочной области относительно изоэлектриче-ской точки, чем в кислой. Согласно уравнению ( 26 - 30), этот случай соответствует величине We ] 32 000 кал / моль. Причина большей устойчивости по отношению к действию отрицательных зарядов неизвестна. Возможно это артефакт, являющийся результатом применения уравнения ( 26 - 30) для вычисления We. Может быть заряды расположены так, что We быстрее возрастает с ростом заряда в кислой области, чем в щелочной. Другая возможность заключается в том, что процесс разворачивания первоначально связан не со всей макромолекулой, а только с ее частью. В этом случае разворачивание начнется, когда Wel любой такой части цепи превысит энергию внутренних связей, и тогда нет никакой необходимости связывать процесс с величиной ] целой макромолекулы. Это будет справедливо, например, если заметный вклад в величину свободной энергии компактной структуры дают водородные связи, в образовании которых принимают участие способные к диссоциации боковые группы. [20]
Страницы: 1 2