Результат - анодный процесс
Cтраница 1
Результаты анодного процесса при электролизе ( выход по току и по веществу в расчете на перхлорат), как это показано Н. А. Изгарышсвым и М. Г. Хачатурян [1], существенно зависят от природы катиона электролита. Чем меньше ионный радиус катиона и больше энергия гидратации его, тем больше должен быть выход по току. Такое представление хорошо согласуется с полученным Н. А. Изгарышсвым и М. Г. Хачатурян экспериментальным материалом при электролизе растворов хлоридов щелочных металлов. [1]
В результате анодного процесса металл разрушается. [2]
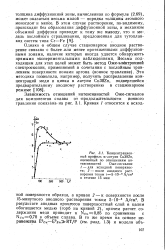
В результате анодных процессов поверхностный слой в целом обогащается медью ( горб на кривой 2), причем расчет содержания меди приводит к NCu 0 85 по сравнению с NC Q70 в объеме сплава. В то же время на основе неравенства E Cu-E znRT / F ( см. разд. [4]
В прианодном слое в результате анодного процесса накапливаются продукты, способные реагировать с органическим веществом. [5]
Электроны, освободившиеся в результате анодного процесса, перемещаются в металле от анодных зон к катодным, где присоединяются к положительно заряженным ионам электролита и нейтрализуют их. [6]
Потери металла при коррозии являются результатом анодного процесса. [7]
Установлено, что полимеризация инициируется в результате анодного процесса. [8]
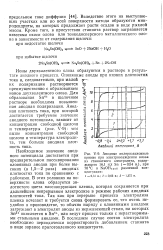 |
Анодные поляризационные кривые при электроосаждении олова из станнатного электролита, содержащего 16 1 г / л Sn ( - 0 54 н., при. [9] |
Ионы двухвалентного олова образуются в растворе в результате анодного процесса. Оловянные аноды при низких плотностях тока и, следовательно, при малой их поляризации растворяются S преимущественно с образованием j ионов двухвалентного олова. Для образования Sn 4 - в щелочном с растворе необходима повышен - ная анодная поляризация. Анод - w ная плотность тока, при которой Е достигается требуемое значение анодного потенциала, зависит от концентрации свободной щелочи и температуры ( рис. V-9): чем выше концентрация свободной щелочи и температура электролита, тем больше анодная плотность тока. [10]
Случаи образования металлорганических соединений при электролизе органических веществ в результате анодных процессов очень редки. [11]
Ионы Двухвалентного Олова образуются в растворе главным образом в результате анодного процесса. Оловянные аноды при низких плотностях тока и, следовательно, при малой поляризации растворяются преимущественно с образованием ионов двухвалентного олова. Для образования ионов Sn4 в щелочном растворе необходима повышенная анодная поляризация. [12]
Следует иметь в виду, что кислотность раствора в результате анодного процесса увеличивается. Это иногда замедляет выделение металла на катоде. [13]
Следует иметь в виду, что кислотность раствора в результате анодного процесса увеличивается. Это иногда замедляет выделение металла на катоде. Так, кадмий выделяется электролизом из слабого сернокислого раствора, однако чрезмерное повышение кислотности препятствует его количественному осаждению. В этом случае необходимо частично нейтрализовать раствор, прибавив, например, ацетат натрия. [14]
Следовательно, не только размер ионного радиуса катиона обусловливает различия в результатах анодного процесса при электросинтезе перхлоратов. [15]
Страницы: 1 2 3