Результат - анодный процесс
Cтраница 2
Следовательно, гетерогенность поверхности металла заключается не в том, что в результате анодного процесса металл на различных участках приобретает различный обратимый потенциал. [16]
Накопление кислоты Каро в растворе невозможно также потому, что она в результате анодного процесса превращается в серную кислоту. [17]
Накопление в электролизуемых растворах кислоты Каро невозможно также потому, что она в результате анодного процесса превращается вновь в серную кислоту. [18]
Протектор является анодом и подвергается интенсивной коррозии, тем самым уменьшая разрушения корпуса аппарата в результате анодных процессов. Аналогичные процессы происходят при катодной защите, когда корпус аппарата присоединяется к отрицательному полюсу источника постоянного тока, а в раствор, содержащийся в аппарате, погружается никелевый стержень, выполняющий роль анода. Для химических аппаратов протекторная защита более удобна в эксплуатации, чем катодная. [19]
Таким образом, установлено, что потеря пластических свойств сталей при коррозии происходит не в результате анодных процессов, а вследствие насыщения стали водородом при катодном процессе. [20]
Так, этилен достаточно быстро и с почти полной конверсией окисляется до углекислого газа и воды на платине, иридии и родии. В результате анодного процесса образуется см есь продуктов неполного окисления: ацетальдегид, ацетон и пропионовый альдегид. [21]
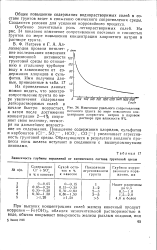 |
Зависимость глубины поражений от химического состава грунтовой среды. [22] |
Повышение содержания хлоридов, сульфатов и карбонатов ( Cl -, SO4 -, НСО, COj) увеличивает агрессивность грунтовой среды. Образующиеся в результате анодного процесса ионы железа вступают в соединение с вышеупомянутыми анионами. [23]
Анализ изменения плотностей коррозионных токов углеродистых сталей при различных напряжениях на основе кривых катодной и анодной поляризации показал, что коррозионная усталость сталей сопровождается увеличением скорости коррозионного процесса на всех этапах разрушения до 1 5 раз. Наибольшее увеличение скорости электрохимической коррозии наблюдается на этапе начального развития микротрещин в результате анодных процессов. Процессы сдвигообразований и развитие магистральной трещины значительно меньше влияют на скорость коррозионного процесса. [24]
А и В; специфической же переменной выступает лишь доля поверхности, занимаемая атомами каждого из компонентов на любой стадии процесса. Если при некотором электродном потенциале для скоростей ионизации чистых компонентов справедливо неравенство IA IB, то в результате анодного процесса на поверхности А В-сплава останутся почти одни только атомы В. [25]
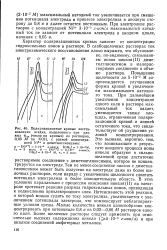 |
Поляризационные кривые восстановления осадка, выделенного при разных фэл ( числа на кривых из растворов, 0 05 М по КОН, с разной концентрацией Ni2 и диметилглиоксима. [26] |
Повышение щелочности до 5 - 10 - 2 М сопровождается улучшением формы кривой и увеличением максимального катодного тока. При дальнейшем увеличении концентрации едкого кали в растворе максимальный ток падает, уменьшается также площадь, ограниченная поляризационной кривой и линией остаточного тока, что свидетельствует об ухудшении условий концентрирования. Это вызвано, вероятно, тем, что возникающие в результате анодного процесса ионы никеля образуют в сильнощелочной среде достаточно растворимое соединение с диметилглиоксимом, которое не концентрируется на электроде. Тем не менее соединение никеля с диметилглиоксимом может быть получено на электроде даже из более щелочных растворов, если наряду с увеличением щелочности сдвигать потенциал электролиза в более положительную область. В этих условиях параллельно с процессом окисления никеля ( II) на электроде протекает реакция разряда гидроксильных ионов, приводящая к подкислению приэлектродного слоя. Интенсивность этой реакции, о которой можно судить по току электролиза, увеличивается с увеличением потенциала электрода, что компенсирует неблагоприятные условия среды. Малые количества никеля целесообразно концентрировать при потенциале 0 8 в из 0 02 - 0 06 М растворов едкого кали. Более щелочные растворы следует применять при относительно высоких содержаниях никеля ( 5 - 10 - 6 г-ион / л) и при анализе соединений амфотерных металлов. [27]
Метод ИВИ весьма избирателен, что обусловлено двумя факторами: селективностью используемого реагента-осадителя и индивидуальными электрохимическими свойствами определяемого элемента. Любые ионы, не образующие нерастворимые соединения в анализируемом растворе и электронеактивные в используемой области потенциалов, не мешают определению. Если концентрирование осуществляется в результате реакции восстановления, определению не мешают элементы-примеси, присутствующие в растворе в низшей валентности. Если концентрирование является результатом анодного процесса, определению не мешают более электроположительные элементы, так как полезная реакция может быть проведена при потенциале, недостаточном для их окисления. [28]
Анодный процесс характеризуется выделением ионов металла трубопроводов в окружающую среду с одновременным выходом из металла свободных электронов. Катодный процесс характеризуется тем, что положительно заряженные ионы металла, соприкасаясь с отрицательно заряженными частицами электролита, образуют нейтральные молекулы. В почвах большой кислотности катодный процесс сопровождается водородной поляризацией с выделением нейтральных атомов и молекул воды. Электроны, освободившиеся в результате анодного процесса, перемещаются в металле от анодных зон к катодным, где присоединяются к положительно заряженным ионам электролита и нейтрализует их. При этом возникает движение электронов - электрический ток коррозии. На всем протяжении трубопроводов возникает множество мелких гальванических пар-элементов, что вызывает разрушение металла и переход его в почву. [29]
На катоде разряжаются только катионы алюминия: А13 Зе - кА1 и, таким образом, для получения металлического алюминия практически расходуется только глинозем. По мере обеднения электролита глиноземом его периодически догружают в ванну. Признаком обеднения электролита служит так называемый анодный эффект, выражающийся в увеличении напряжения с 4 - 4 5 до 25 - 30 В. Отрицательно заряженные анионы АЮз - направляются к аноду; в результате анодного процесса 2А1О - - 6е - А12Оз 11 / 2О2 выделяется газообразный кислород, вызывающий постепенное сгорание угольных анодов. [30]
Страницы: 1 2 3