Диметилпентан
Cтраница 1
Диметилпентан ( триметилпропилметан) был также23 подвергнут нитрованию и дал при этом 2 2-диметил - З - нитропентан ( d 0 9520, темп. [1]
Диметилпентан приблизительно на 23 % изомеризуется в 2 3-диметилпентан и приблизительно на 23 % превращается в продукты алкилированияидиспро-порционирования. [2]
 |
Хроматограмма фракции н. к. - 125 С нефти Самотлорского месторождения ( неподвижная фаза - сквалан, 50 С. [3] |
Диметилпентан; П - 1 1-диметилпентан; / 8 - Я-метилгексан; 19 - 1 3-цис-диметилциклопентан; 20 - 1 3-гранс-диметилциклопентан; 21 - 1 2-т-ранс - диметилциклопентан 3-этилпентан; 22 - к-гептан; 23 - 1 2-цис-диметилцикло - пентан 2 2-диметилгексан; 24 - 1 1 3-триметилциклопентан; 25 - метилциклогексан; 26 - 2 5-диметилгексан; 27 - 2 4 - ДИметилгексан; 28 - этилциклопентан; 29 - 2 2 3-триметилпен-тан; 30 - 1 2 4-гранс. [4]
ДИметилпентан; в - цик - ПрОСТОЙ графический Мб - логексан; г - метилциклопентан, и-гексан. [5]
Диметилпентан, 2 3-диметюшентан и 3-этилпентан способны только к Cs-дегидроциклизации и, следовательно, их ароматизирующая способность в основном должна определяться реакциями II и III. На образце катализатора с большей кислотностью выход алкилциклопентанов достигает максимума в области температур 430 - 460 С и при дальнейшем ее повышении резко снижается, что, по мнению автора, связано с заметным участием пятичленных цикланов в образовании толуола путем их дегидроизомеризации. [6]
Однако при 120 образование диметилпентанов происходит в небольшой степени, а количество образующегося 2-метилгексана значительно ниже того количества, которое соответствует равновесному значению. [7]
 |
Хроматограммы фракций С5, С6, С полученные с помощью двухстадийной газо-жидкост. [8] |
Л-22 - и 2 4 - ДИметилпентан; / 2 - 3 3-дяметилп снтан; 13 - 2-метнлгексан; 14 - 2 3-диметилпсн-тан 3-метилгексая; 15 - 1 1-дииетилциклопентан и 3-этил-пеытан; If-шранс - 1 3-днметилдиклопситан; 17-н-пптан; / S-транс - 1 2-дпциклопентан; / 9-цис - l 2-диметилцикло-пентан; 20-метилциклогексан; 2 / - этилциклопентан; 22 - толуол при 195 мин. [9]
Во всяком случае, отделение циклогексана от двух диметилпентанов легко достигается с помощью азеотропной перегонки. [10]
С еще меньшей скоростью из смеси метил - и диметилпентанов образуются 2 2-диметилбутан и я-гексан; константы скорости их образования примерно на два порядка ниже, чем константа скорости второй стадии. Определенные в работе [14] кинетические параметры приведены в табл. III.6. Низкие энергии активации для миграции метального радикала привели к выводу, что эта стадия, в отличие от других, тормозится массопередачей. Однако экспериментально роль мас-сопередачи подтверждена не была. [11]
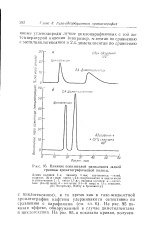 |
Влияние понизителей размывания задней границы хроматографической полосы. [12] |
На рис. 95 показан эффект, обнаруженный в случае диметилпентана и циклогсксана. [13]
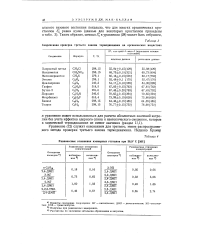 |
Современная проверка третьего закона термодинамики на органических веществах. [14] |
Приняты следующие сокращения: МГ - метилгексан; ДМП - диметилпентан; ЭП - этилпен - - тан; ТМБ - триметилбутан. [15]
Страницы: 1 2 3