Молекулярный вес - кислота
Cтраница 1
Молекулярный вес кислоты может быть определен на основании числа нейтрализации или кислотного числа (, ), которое равно количеству миллиграммов едкого кали, израсходованного на нейтрализацию 1 г кислоты или смеси кислот. [1]
Молекулярный вес кислоты определен путем титрования 1 / 10 N раствором едкого натра. [2]
Молекулярный вес кислот, вычисленный по результатам титрования, как правило, был выше молекулярного веса, полученного при омылении. Это может-быть объяснено тем, что непредельные метилкетоны в процессе окисления превращаются в оксикислоты, которые, в результате дальнейших превращений, в условиях титрования не могут быть обнаружены. [3]
Молекулярный вес асфальтогсновых кислот показывает, что они образовались в результате соединения двух молекул высококипящего углеводорода. [4]
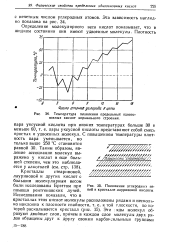 |
Положение углеродных це-пей в кристалле лауриновой кислоты. [5] |
Определение молекулярного веса кислот показывает, что в жидком состоянии они имеют удвоенные молекулы. [6]
Определения молекулярного веса кислот криоскопическим методом в некоторых растворителях ( в бензоле или хлороформе), а также определение плотности паров, например уксусной кислоты, показывают, что кислоты образуют молекулы состава ( СЛН2 О2) 2 с удвоенным против формулы строения молекулярным весом. [7]
Определения молекулярного веса кислот криоскопическим методом в некоторых растворителях ( в бензоле или хлороформе), а также определение плотности паров, например уксусной кислоты, показывают, что кислоты образуют молекулы состава ( СЛН2ЛО2) 2 с удвоенным против формулы строения молекулярным весом. [8]
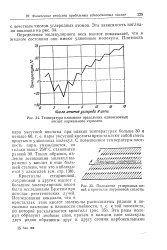 |
Температура плавления предельных одноосновных кислот нормального строения.| Положение углеродных цепей в кристалле лауриновой кислоты. [9] |
Определение молекулярного веса кислот показывает, что в жидком состоянии они имеют удвоенные молекулы. [10]
Определения молекулярного веса кислот криоскопическим способом в некоторых растворителях, как, например, в бензоле или хлороформе, а также определение плотности паров, например, уксусной кислоты, показывают, что кислоты образуют молекулы состава ( СгаН2га02) 2 с удвоенным против формулы строения молекулярным весом. [11]
С увеличением молекулярного веса кислоты выход диацилатов дифенилсвинца уменьшается. Диацилаты диарилсвин-ца и высших карбоновых кислот обычно получают реакцией переацидирова-ния ( см. стр. [12]
С понижением молекулярного веса кислот растворимость их солей в топливах ухудшается. Нерастворимые соли отлагаются на стенках тары или остаются во взвешенном состоянии. [13]
С увеличением молекулярного веса кислот повышается - их температура кипения и уменьшается плотность. [14]
Поэтому при незначительном молекулярном весе кислот, образующихся при окислении циклогексана, реакция ( VI, 24) является единственной, с которой приходится считаться, рассматривая возможные окислительные превращения кислот. [15]
Страницы: 1 2 3 4