Рекомбинация - радикал
Cтраница 3
При рекомбинации радикалов время жизни R - ( 1Д2) может быть в сотни и тысячи раз больше и &3 [ М ] значимо уже при умеренных давлениях. [31]
 |
Энергии гемолитической диссоциации связей в молекулах некоторых соединений [ 30, с. 21 ]. [32] |
При рекомбинации радикалов с образованием молекулы выделяется столько же энергии, сколько необходимо для ее диссоциации на радикалы. [33]
При рекомбинации радикалов и их взаимодействии с двойными связями происходит сшивание макромолекул. [34]
Одновременно рекомбинация цепных радикалов на стадии обрыва цепи может вызывать образование в полимерной структуре поперечных связей. [35]
При рекомбинации алл ильных радикалов образуется дополнительное количество сшивок. До на чала гелеобразования образования аллильных радикалов при облучении полипропилена не происходит и, следовательно, дополнительное образование сшивок отсутствует. [36]
 |
Энергии активации реакций распада радикалов.| Соотношение для оценки энергии активации различных типов реакций. [37] |
Реакции рекомбинации радикалов протекают практически с нулевой энергией активации; как следствие, обратные им реакции образования радикалов с разрывом С-С - или С - Н - свя-зи в молекулах протекают с энергией активации, равной энергии разрыва соответствующей связи. [38]
Вероятность рекомбинации радикалов значительно возрастает благодаря повсеместному присутствию молекул воды, обеспечивающих тройные удары, а также возрастает по механизму Франка-Рабиновича [21] возможность непосредственной рекомбинации радикалов, образующихся из одной и той же молекулы воды при ее диссоциации в результате электронного удара. Наконец, в жидкости продолжительность жизни любой возбужденной частицы должна быть много меньше, чем в газовой фазе. Все эти эффекты целесообразно рассматривать в зависимости, во-первых, от природы, числа и пространственного распределения образующихся радикалов и, во-вторых, от различных возможных механизмов их взаимодействия с другими молекулами и свободными радикалами. [39]
Скорость рекомбинации радикалов равна 2 / с8 [ R12, где ks - константа скорости рекомбинации, л / молъ сек; [ R ] - молярная концентрация радикалов R. Скорость реакции ( 9) равна k9 [ R ] [ S ], где &9 - константа скорости реакции ( 9); [ S ] - молярная концентрация S. Радикалы R образуются со скоростью, пропорциональной мощности дозы. Она, очевидно, равна GR ( 7 / 100 дг), где GR - выход радикалов; / - мощность поглощенной дозы, зв / л-сек; JV - число Авогадро. Скорости образования и исчезновения радикалов должны быть равны. [40]
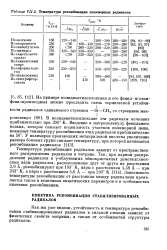 |
Температура рекомбинации полимерных радикалов. [41] |
Температура рекомбинации радикалов зависит от пространственного распределения радикалов в матрице. Зависимость температуры рекомбинации от расстояния между радикалами проявляется также в величинах кинетических параметров и в особенностях кинетики рекомбинации. [42]
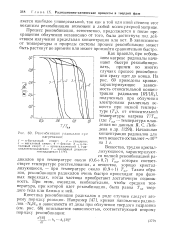 |
Рекомбинация радикалов при нагревании. [43] |
Кинетика рекомбинации радикалов в ряде случаев следует второму порядку реакции. [44]
Кинетика рекомбинации радикалов в некоторых случаях подчиняется простым порядкам реакции. [45]
Страницы: 1 2 3 4