Замедленная рекомбинация
Cтраница 1
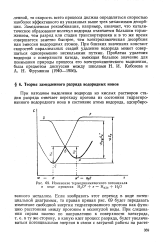 |
Изменение термодинамического потенциала в ходе процесса Н3О е Надо Н2О. [1] |
Замедленная рекомбинация, например, означает, что каталитическое образование молекул водорода отличается большим торможением, чем разряд или стадия транспортировки и в то же время совершается заметно быстрее, чем электрохимическая десорбция или эмиссия водородных атомов. При близких значениях констант скоростей параллельных стадий удаление водорода может совершаться одновременно несколькими путями. [2]
При замедленной рекомбинации для протекания реакции выделения водорода с заданной скоростью на поверхности металла необходим избыток водородных атомов по сравнению с равновесными условиями. [3]
По теории замедленной рекомбинации для тех случаев, когда адсорбция водорода незначительна и поверхность катода энергетически однородна, величина ( 3 должна равняться единице. В условиях заметной адсорбции водорода р может принимать любые значения, лежащие между нулем и единицей. Если же опытная величина b равна или близка к 0 12 и водород почти не адсорбируется на поверхности катода, то это указывает на замедленность разряда. [4]
Согласно теории замедленной рекомбинации для тех случаев, когда адсорбция водорода незначительна и поверхность катода энергетически однородна, величина р должна равняться единице. В условиях заметной адсорбции водорода р может принимать любые значения, лежащие между нулем и единицей. [5]
В отличие от теории замедленной рекомбинации в ее первом варианте, где коэффициент Ь при заданной температуре был некоторой константой, одинаковой для всех металлов, здесь он уже является функцией природы металла и в зависимости от величины Р может принимать различные значения. Это уточнение не сказывается, однако, на форме уравнения ( 642), которое остается таким же, как и в первоначальной теории. [6]
В таком виде теорию замедленной рекомбинации следует рассматривать как первое приближение к реально существующим соотношениям. Это первое приближение отвечает идеализированному случаю, когда поверхность катода энергетически однородна, и между адсорбированными атомами водорода полностью отсутствуют силы взаимодействия. В реальных условиях выделения водорода эти допущения могут и не оправдываться, что должно изменять соотношения между потенциалом и плотностью тока. [7]
В отличие от теории замедленной рекомбинации в ее первом варианте, где коэффициент b при заданной температуре был некоторой константой, одинаковой для всех металлов, здесь он уже является функцией природы металла и в зависимости от величины р может принимать различные значения. Это уточнение не сказывается, однако, на форме уравнения ( XV-31), которое остается таким же, как и в первоначальной теории. [8]
В таком виде теорию замедленной рекомбинации следует рассматривать как первое приближение к реально существующим соотношениям. Это приближение отвечает идеализированному случаю, когда поверхность катода энергетически однородна и между адсорбированными атомами водорода полностью отсутствуют силы взаимодействия. В реальных условиях выделения водорода эти допущения могут и не оправдываться, что должно изменять соотношения между потенциалом и плотностью тока. [9]
В отличие от теории замедленной рекомбинации в ее первом варианте, где коэффициент b при заданной температуре был некоторой константой, одинаковой для всех металлов, здесь он уже является функцией природы металла и в зависимости от ( 3 может принимать различные значения. Это уточнение не сказывается, однако, на форме уравнения (19.32), которое остается таким же, как и в первоначальной теории. [10]
В таком виде теорию замедленной рекомбинации следует рассматривать как первое приближение к реально существующим соотношениям. Это приближение отвечает идеализированному случаю, когда поверхность катода энергетически однородна и между адсорбированными атомами водорода полностью отсутствуют силы взаимодействия. В реальных условиях выделения водорода эти допущения могут и не оправдываться, что должно изменять соотношения между потенциалом и плотностью тока. [11]
В отличие от теории замедленной рекомбинации в ее первом варианте, где коэффициент b при заданной температуре был некоторой константой, одинаковой для всех металлов, здесь он уже является функцией природы металла и в зависимости от р может принимать различные значения. Это уточнение не сказывается, однако, на форме уравнения ( 19.32), которое остается таким же, как и в первоначальной теории. [12]
Изучение кинетических токов, обусловленных замедленной рекомбинацией частиц, было начато Брдичкой и Визнером [3], исследовавшими электродные реакции рекомбинации анионов кислот. [13]
Эквивалентная цепь переменного тока для механизма замедленной рекомбинации формально будет совпадать с эквивалентной цепью в случае механизма электрохимической десорбции. [14]
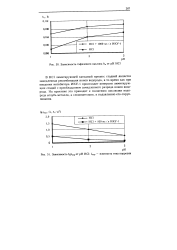 |
Зависимость тафелевого наклона Ьк от рН НС1.| Зависимость 1 % гкорот рН НС1. г кор - плотность тока коррозии. [15] |
Страницы: 1 2 3 4