Четырехвалентный рений
Cтраница 1
 |
Потенциалы ионизации рения и некоторых сходных с ним элементов. [1] |
Четырехвалентный рений образуется в водных растворах в присутствии различных комплексообразующих веществ и избытка восстановителей. [2]
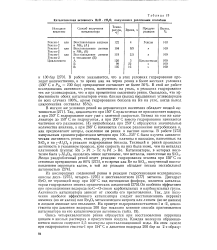 |
Каталитическая активность ReO 2Н20, полученного различными способами. [3] |
Окись четырехвалентного рения образуется при восстановлении перрената цинком в кислых растворах в присутствии воздуха. Каждая молекула образовавшегося окисла содержит 2 5 молекулы кристаллизационной воды. [4]
Структурный материал по соединениям четырехвалентного рения весьма беден. Во всех соединениях металл имеет окта-эдрическую координацию: в калиевом и n - толуидиниевом гек-сахлорренатах и в гранс-дихлоро-бис-ацетилацетонате в виде мономерных комплексов, в K CbReOReClsJI O в виде дву-ядерных комплексов с линейным кислородным мостиком, в ReCl4 в виде двуядерных фрагментов Re2Clg ( два сопряженных по общей грани октаэдра), связанных в цепи мостиковы-ми атомами хлора, и, наконец, в ReSe2 в виде искаженной гексагональной упаковки атомов Se с послойным заполнением атомами Re половины октаэдрических пустот. [5]
Известны многочисленные устойчивые соединения электроположительного четырехвалентного рения. [6]
Двуокись и дисульфид рения содержат четырехвалентный рений, способный окисляться до семивалентного с образованием растворимых соединений. Окислителем может быть реагент с потенциалом выше потенциала системы ReIV / Revn 0 51 В. Четырехвалентный рений образует ряд растворимых комплексов с галогенами, роданидом, тиокарбаматом и сульфитом. [7]
При дальнейшем титровании происходит восстановление четырехвалентного рения, но скачок потенциала не наблюдается. [8]
Так, например, при облучении хлорида четырехвалентного рения нейтронами было обнаружено образование иона перрената. При облучении гидратов солей трехвалентного хрома было найдено, что до 10 % радиоактивного хрома оказываются в шестивалентном состоянии. [9]
Вещество быстро восстанавливается многими органическими соединениями до соединений четырехвалентного рения. [10]
Для семи -, шести -, пяти - и четырехвалентного рения получены некоторые фториды и оксифториды. Все фториды и оксифториды легко возгоняются при низких температурах [ 1149, 1150, 12301 и легко гидролизуются водой. [11]
Метод основан на восстановлении солями хрома ( II) перрената до четырехвалентного рения. Точку эквивалентности устанавливают с помощью компенсационного потенциометра, применяя в качестве индикаторного электрода платиновую пластинку, а в качестве электрода сравнения - насыщенный каломельный полуэлемент. Определение возможно в присутствии небольших количеств молибдена ( Re: Mo Г: 1), а также-железа, титана, хрома, ванадия, никеля, кобальта, ниобия и меди. Последние легко отделяются в виде гидроокисей путем осаждения аммиаком или щелочью перед титрованием. [12]
Кроме этого, описаны соли, отвечающие пятивалентному рению ( желтые гипоренаты), и коричневые рениты MejReOj - производные четырехвалентного рения. [13]
Экстрагируют Mo ( VI) из 6 7VHC1 амилацетатом или диэтиловым эфиром. Четырехвалентный рений остается в водной фазе. [14]
Также диамагнитен Na2 [ ReO3 ] или ыть может слегка парамагнитен, хотя данное соединение, пови-имому, имеет нечетное число электронов. Дру-ие соединения четырехвалентного рения, как, например, yReCl6 ], Ag2 [ ReCl6 ] и K2 [ ReBr6 ], являются парамагнитными и меют моменты, равные примерно 3 2 магнетона Бора. [15]
Страницы: 1 2