Более низкое значение - энергия - активация
Cтраница 1
Более низкие значения энергии активации для цетановых чисел по сравнению с аналогичными показателями для октановых чисел [43], очевидно, связаны с различной характеристикой термической стабильности углеводородных структур топлив для двигателей с искровым зажиганием и дизелей. [1]
При этом наблюдаются более низкие значения энергии активации ( примерно на 10 ккал / моль меньше, чем у эфиров двухосновных кислот), а метоксильная группа обладает аномально высокой реакционной способностью. Это различие в реакционной способности однотипных С - Н связей разных эфиров нельзя объяснить прочностью этих связей, так как она должна быть одинаковой. Наиболее вероятной причиной является разная квадрупольная структура переходного состояния при атаке кумилпероксирадикала на С - Н связь эфира одноосновной и двухосновной ( содержащей две полярные группы) кислот. [2]
Аппена [155, 163], обеспечивают образование химических связей большей прочности в условиях более низких температур и при более низких значениях энергии активации. [3]
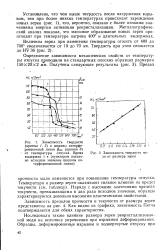
Установлено, что чем выше твердость после нагружения взрывом, тем при более изких температурах происходит зарождение новых зерен ( рис. 1), что, вероятно, связано с более низкими значениями энергии активации рекристаллизации. Металлографический анализ показал, что массовое образование новых зерен происходит при температуре нагрева 400 и длительных выдержках. [5]
Применение более низких значений энергий активации элементарных реакций развития цепи в прежних радикально-цепных схемах разложения этана не приводит уже к первому порядку кинетики распада, хотя несколько сближает вычисленную и измеренную концентрации радикалов. Правильной следует считать только ту радикально-цепную схему, в которой отражено самоторможение ( или торможение) и лишь при экстраполяции к х О получается первый порядок. [6]
Делокализация электронов часто является причиной стабилизации системы. Такая стабилизация соответствует более низкому значению энергии активации, так что мы можем характеризовать ( с некоторыми оговорками, сделанными в предыдущем параграфе) относительную скорость реакции с помощью величины этой энергии стабилизации. [7]
В кристаллических полимерах отрезки макромолекул, находящиеся в аморфной фазе и принимающие участие в сегментальной подвижности, в значительной мере ограничены в движении из-за наличия кристаллической фазы, поэтому чрезмерного увеличения кооперативно-сти в движении не наблюдается. Этот факт, в частности, подтверждается более низким значением энергии активации дипольно-сегментальной релаксации и электропроводности при ТТС в кристаллических полимерах по сравнению с соответствующими аморфными. [8]
В частично кристаллических полимерах участки макромолекул, находящиеся в аморфной фазе и принимающие участие в сегментальной подвижности, в значительной мере ограничены в движении, и чрезмерного увеличения кооперативное в движении не наблюдается. Этот факт, в частности -, подтверждается более низким значением энергии активации дипольно-сегментальной релаксации и электропроводности при ТТС в кристаллических полимерах по сравнению с аморфными. [9]
Скорость растворения арсенида галлия также в основном определяется скоростью химической реакции на поверхности монокристалла с энергией активации около 12 ккал / моль. В отличие от германия и арсенида галлия растворение антимонида галлия происходит с более низкими значениями энергии активации и возрастает в перемешиваемом растворе по сравнению с неподвижным. Величина пэ Ж - Приведенные данные свидетельствуют о лимитировании процесса растворения GaSb диффузией в растворе. [10]
О влиянии процесса диффузии на скорость растворения стекол № 2 - 7 свидетельствуют и более низкие значения энергии активации растворения ( 10 ккал / моль) в неперемешиваемых растворах. [11]
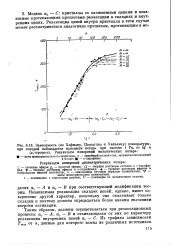 |
Зависимость ( по Хофману, Пассаглиа и Уильямсу температуры, при которой наблюдается максимум потерь при частоте 1 Гц, от lg п. [12] |
Независимая релаксация складок цепей, однако, имеет совершенно другой характер, поскольку она охватывает только складки и поэтому должна определяться более низким значением энергии активации. [13]
Температура влияет также на вторичные реакции превращения алкенов. Распад алкенов, протекающий с высокими энергиями активации, значительно ускоряется с повышением температуры по сравнению с реакциями конденсации алкенов, характеризующимися более низкими значениями энергии активации. [14]
Температура влияет также на вторичные реакции превращения алкенов. Распад алкенов, протекающие с высокими энергиями активации, значительно ускоряется с повышением температуры по сравнению с реакциями конденсации алкенов, характеризующимися более низкими значениями энергии активации. [15]
Страницы: 1 2