Ретинальдегид
Cтраница 2
В экстремальных случаях недостатка витамина А ( ретинола) запасы в печени истощаются, и, хотя снабжение сетчатки поддерживается до последней возможности, в конце концов может образоваться его дефицит. В результате организму не удается восполнять потери ретинальдегида и, следовательно, регенерировать зрительный пигмент. Наступает слепота, вначале обратимая, но при длительном дефиците ретинола переходящая в постоянную из-за денатурации опсина, нестабильного в свободном состоянии. А - - ( 3-кароти-на и таким образом помогает предотвратить недостаточность витамина А и вызываемую этой недостаточностью слепоту. [16]
У некоторых видов земноводных и рыб ретинол может превращаться в 3 4-дидегидроретинол ( или наоборот), в результате чего пигмент в рецепторе изменяется с родопсина на пор-фиропсин. Опсин в рецепторе может соединяться с 11-цыс-изо - мером как ретинальдегида, так и 3 4-дидегидроретинальдегида, и, следовательно, тип образующегося зрительного пигмента зависит от того, какой хрохмофор присоединен к опсину. По-видимому, должны существовать механизмы, с помощью которых пигментный эпителий может осуществлять взаимопревращения этих двух ретинолов, а также выбирать правильный ретинол, необходимый в данном конкретном случае. [17]
Процесс зрения зависит от группы фоточувствительных пигментов, которые локализованы в сетчатке глаза. Эти зрительные пигменты представляют собой комплексы опсинов ( глико-липопротеинов) и 11 - ис-ретинальдегида или 11-цис-дегидро - ретинальдегида. Более детально эти комплексы и их функции в процессе зрения обсуждаются в гл. [18]
Для транспорта ретинола в сетчатку глаза используется специфический ли-попротеин - ретинолсвязывающий белок. В сетчатке ретинол может превращаться в ретинальдегид и включаться в состав зрительных пигментов. [19]
Почти все исследования по связыванию ретинальдегида л опсина были проведены с родопсином, выделенным из палочек сетчатки позвоночных, главным образом на примере крупного рогатого скота. По-видимому, другие зрительные пигменты в основном сходны с этим родопсином. Необходимо рассмотреть два вида связывания - первичное связывание, с помощью которого ретинальдегид ковалентно присоединяется к функциональной группе опсина, и вторичное, обусловленное нековалент-ными взаимодействиями. [20]
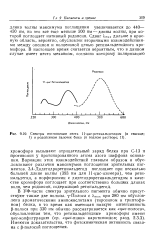 |
Спектры поглощения света И - ис-ретинальдегидом ( в гексане. / и родопсином палочек быка ( в водном растворе. II. [21] |
С-13 и противоион у протонированного атома азота шиффова основания. Вариации этих взаимодействий главным образом и обусловливают различия максимумов поглощения зрительных пигментов. Дидегидроретннальдегид поглощает при несколько большей длине волны ( 393 нм для И-цис-изомера), чем рети-нальдегид, а порфиропсин с дидегидроретинальдегидом в качестве хромофора поглощает при соответственно больших длинах волн, чем родопсин, содержащий ретинальдегид. [22]
Ферментативное восстановление транс-ретинальдегида до транс-ретинола, катализируемое алкогольдегидрогеназой, происходит в рецепторной мембране, и для него необходим NADH. Ретинол транспортируется из рецепторной клетки в пигментный эпителий, где он может этерифицироваться жирными кислотами, главным образом пальмитиновой и стеариновой. Ретинол и ретиниловые эфиры, образовавшиеся из зрительных пигментов вместе с запасными, сохраняющимися в пигментном эпителии, образуют внутриклеточный фонд. Изомеризация ретинола, ретинальдегида и ретиниловых эфиров до ыс-11 - формы продемонстрирована в эксперименте. Расщепление ыс-ретини-ловых эфиров ( где происходит этот процесс, пока не известно) дает 11 - ыс-ретинол, который может быть снова окислен в рецепторе до альдегида. Полагают, что рекомбинация 11 - нс-ре-тинальдегида с опсином происходит спонтанно. [23]
Страницы: 1 2