Диметилфумарат
Cтраница 1
Диметилфумарат Диметилсукцннат Днэтилоксалат Хлористый бепзи. Бромтолуол о - Бромтолуол / г - Бромтолуол Хлористый бенз. [1]
Особо рекомендуемый диметилфумарат может найти лишь ограниченное применение вследствие присущей ему летучести. [2]
В случае стирола, диметилфумарата и 1 4-бензохинона он осуществил реакцию при умеренной температуре и установил, что первоначально образуется 1-фенил - 4 5-ди-гидро - 1 2 3-триазол. Три указанных выше соединения содержат одну или две соседние с двойной связью активирующие группы. [3]
Примечательно, что присоединение метилдиазоацетата к диметилфумарату или диметилмалеату дает один и тот же продукт. [4]
Однако р-фенилметилакрилат, так же как и диметилфумарат, недостаточно летуч для того, чтобы его можно было определить с помощью масс-спектрометра без обогреваемой системы напуска. Поэтому на рис. НО указаны только два продукта. Пунктирная линия относится к метилакрилату, сплошная - к стиролу. Экспериментальные точки достаточно хорошо совпадают с этими теоретическими кривыми. [5]
Обсудите возможные причины появления дипольного момента у диметилфумарата ( 2 25 Д в ССЦ) и сравните его с рассчитанными по аддитивной схеме для плоских конформеров и для случая свободного вращения карбометоксигрупп. [6]
Кроме того, с выходом 15 % была получена смесь диметилфумарата и ди-метилацетата. [7]
Смесь 60 г ( 0 314 моль) свежеперегнанного диенина и 10 г ( 0 07 моль диметилфумарата нагревали в запаянной стеклянной ампуле 24 ч при температуре 175 С в атмосфере азота. [8]
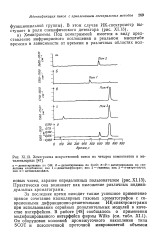 |
Хемиграмма искусственной смеси из четырех компонентов в ме-тиленхлориде. [9] |
ОН; б - детектирование по СО; в-д - детектирование по скелетным колебаниям; пик 1 - диметилфумарат; пик 2 -гваякол - пик 3 - о-нитротолуол-пик 4 - ыетилсалицилат. [10]
Этот карбен в противоположность электрофильным дигалогенкарбенам легко присоединяется к олефинам, содержащим электроноакцепторные заместители, таким, как акрилонитрил, этилакрилат, диметилфумарат, образуя с удовлетворительными выходами ( 25 - 73 %) соответствующие функционально замещенные циклопропаны. [11]
Металлалкильные интермедиаты были также выделены [30] при присоединении ( n - CsHs) 2МоН2 [ или ( cp MoHj ] к ненасыщенным сложным эфирам, таким как диметилфумарат или малеат. [12]
Хиндерзин и Лудингтон [19] с помощью газовой хроматографии проводили детальные анализы продуктов реакции три-метилфосфита с диметиловыми эфирами фумаровой и малеи-новой кислот, причем кроме указанных исходных веществ определялось содержание продуктов реакции диметилового эфира метилфосфиновой кислоты, диметилфумарата ( малеата), диметилового эфира диметилфосфорянтарной кислоты. [13]
Диаминобутадиены-1 3 тоже способны к диеновым конденсациям. Его аддукт с диметилфумаратом не был выделен, а при конденсации с малеиновым ангидридом и бутилвиниловым эфиром образуются лишь полимерные продукты. [14]
Интересно отметить также более высокую реакционную способность транс-алкенов по сравнению с соответствующими ис-изомерами. Коэффициенты относительных скоростей для диметилфумарата и малеата отличаются в 36 раз, в то время как тране-стильбен взаимодействует в 26 раз быстрее, чем мс-соединение. На первый взгляд эти данные кажутся неожиданными, так как более богатый энергией малеат присоединяет бром или сульфнт-пон быстрее, чем фумарат. Валентные углы в 120 при двух р2 - гибриднзованных центрах могут вызывать значительное вандерваальсовское сжатие ( fuc - заместителей в основном состоянии. Кроме того, в ходе многоцентрового процесса хра-центры должны переходить в хра-гибридизованное состояние. Соответствующее сокращение валентных углов вызывает повышение пространственного взаимодействия заслоненных ис-заместителей, несмотря на некоторое удлинение углерод-углеродной связи, соединяющей два тетраэдрических атома. [15]
Страницы: 1 2