Рецептор - гормон
Cтраница 2
Аналогичная проблема возникает в случае инсулина. В растворе гексамер инсулина находится в равновесии с димерами и мономерами. Поскольку димер, по-видимому, важен для связывания с рецепторами гормона, его необходимо идентифицировать. Судя по величинам, приведенным в табл. 5.5, прочность обоих возможных димеров не должна сильно различаться. Однако димер ОР помимо несколько более прочного контакта образует антипараллельную ( 3-структуру. [16]
Рецепторы, будучи первичными приемниками внеклеточных сигналов, гибко реагируют на их интенсивность. Они являются регуляторными белками, и на их активность влияют различные факторы типа тех, которые были обсуждены выше. Суммируя механизм регуляции, можно сказать, что активность рецепторов, включая рецепторы гормонов и медиаторов, регулируется, во-первых, числом рецепторов и, во-вторых, их сродством к эффекторам. [17]
В настоящее время получены доказательства, что это действие осуществляется через так называемые гормональные рецепторы, под которыми понимают химические структуры соответствующих тканей-мишеней, содержащие высокоспецифические участки ( углеводные фрагменты гликопротеинов и ганглиозидов) для связывания гормонов. Результатом подобного связывания является инициация рецепторами специфических биохимических реакций, обеспечивающих реализацию конечного эффекта соответствующего гормона. Рецепторы гормонов белковой и пептидной природы расположены на наружной поверхности клетки ( на плазматической мембране), а рецепторы гормонов стероидной природы-в ядре. Общим признаком всех рецепторов независимо от локализации является наличие строго пространственного и структурного соответствия между рецептором и соответствующим гормоном. [18]
В настоящее время получены доказательства, что это действие осуществляется через так называемые гормональные рецепторы, под которыми понимают химические структуры соответствующих тканей-мишеней, содержащие высокоспецифические участки ( углеводные фрагменты гликопротеинов и ганглиозидов) для связывания гормонов. Результатом подобного связывания является инициация рецепторами специфических биохимических реакций, обеспечивающих реализацию конечного эффекта соответствующего гормона. Рецепторы гормонов белковой и пептидной природы расположены на наружной поверхности клетки ( на плазматической мембране), а рецепторы гормонов стероидной природы-в ядре. Общим признаком всех рецепторов независимо от локализации является наличие строго пространственного и структурного соответствия между рецептором и соответствующим гормоном. [19]
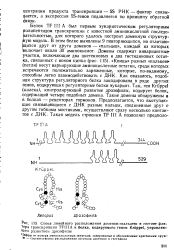 |
Схема линейного расположения доменов-пальцев в составе фактора транскрипции TFIIIA и белка, кодируемого геном Kruppel, управляющим развитием дрозофилы. [20] |
В этом белке выявлены 9 повторяющихся, но отличаются друг от друга доменов - пальцев, каждый из которых включает около 30 аминокислот. Концы разных пальцев ( петли) несут варьирующие аминокислотные остатки, среди которых встречаются положительно заряженные, которые, по-видимому, способны легко взаимодействовать с ДНК - Как оказалось, подобная структура регуляторного белка закодирована в ряде других генов, кодирующих регуляторные белки эукариот. Так, ген Kruppel ( калека), контролирующий развитие дрозофилы, кодирует белок, содержащий четыре подобных домена. Такие домены обнаружены и в белках - рецепторах гормонов. Предполагается, что выступающие связывающиеся с ДНК разные пальцы, соединенные друг с другом гибкими мостиками, осуществляют сразу несколько контактов с ДНК. [21]
Если постсинаптическая мембрана подвергается действию увеличенных концентраций ацетилхолина ( и если одновременно блокируется ацетилхолинэстераза), то наблюдается медленное снижение постсинаптичеокого ответа. По-видимому, мембрана становится менее чувствительной к агонистам. Это явление, называемое десенсибилизацией, наблюдается на всех трех уровнях организации: в интактной ткани, в мембранных везикулах и в изолированном рецепторе. Ионный поток через мембрану ин-гнбируется, но не потому, что рецепторы связывают агонисты слабее, а потому, что ионные каналы не открываются. Фармакологическая десенсибилизация наблюдается не только для аце-тилхолинового рецептора, но и для многих других систем, например для рецепторов пептидных гормонов и 3-адренэргиче-ских рецепторов. [22]
 |
Схема линейного расположения доменов-шальцев в составе фактора транскрипции TFIIIA и белка, кодируемого геном Kruppel, уггравляю. [23] |
В этом белке выявлены 9 повторяющихся, но отличаю-шихся друг от друга доменов - пальцев, каждый из которых включает около 30 аминокислот. Концы разных пальцев ( петли) несут варьирующие аминокислотные остатки, среди которых встречаются положительно заряженные, которые, по-видимому, способны легко взаимодействовать с ДНК. Как оказалось, подобная структура регуляторного белка закодирована в ряде других генов, кодирующих регуляторные белки эукариот. Так, ген Kruppel ( калека), контролирующий развитие дрозофилы, кодирует белок, содержащий четыре подобных домена. Такие домены обнаружены и в белках - рецепторах гормонов. Предполагается, что выступающие связывающиеся с ДНК разные пальцы, соединенные друг с другом гибкими мостиками, осуществляют сразу несколько контактов с ДНК. [24]
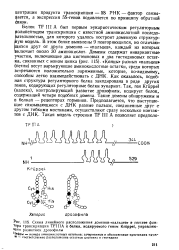 |
Схема линейного расположения доменов-пальцев в составе фактора транскрипции TFIIIA и белка, кодируемого геном Kruppel, управляю. [25] |
В этом белке выявлены 9 повторяющихся, но отличающихся друг от друга доменов - пальцев, каждый из которых включает около 30 аминокислот. Концы разных пальцев ( петли) несут варьирующие аминокислотные остатки, среди которых встречаются положительно заряженные, которые, по-видимому, способны легко взаимодействовать с ДНК. Как оказалось, подобная структура регуляторного белка закодирована в ряде других генов, кодирующих регуляторные белки эукариот. Так, ген Kruppel ( калека), контролирующий развитие дрозофилы, кодирует белок, содержащий четыре подобных домена. Такие домены обнаружены и в белках - рецепторах гормонов. Предполагается, что выступающие связывающиеся с ДНК разные пальцы, соединенные друг с другом гибкими мостиками, осуществляют сразу несколько контактов с ДНК. [26]
Страницы: 1 2