Максимальное значение - энтропия
Cтраница 2
Система в основном находится в равновесном состоянии, отвечающем максимальному значению энтропии системы; отклонившись от этого состояния, система затем возвращается к нему. При наблюдении системы продолжительное время можно отметить, что случаи увеличения и уменьшения энтропии встречаются одинаково часто, причем время повторяемости какого-либо отклонения системы от равновесного состояния тем больше, чем меньше вероятность данного неравновесного состояния. С увеличением размеров системы время повторяемости быстро возрастает. Поэтому процессы, являющиеся необратимыми с точки зрения обычной термодинамики, представляются практически необратимыми и со статистической точки зрения. Указанное обстоятельство сближает обе формулировки второго начала термодинамики и практически снимает отмеченное выше и различие. [16]
Докажем для простейшего случая ( для однофазной системы), что максимальное значение энтропии или минимальное значение свободной энергии системы соответствуют равнораспределению изотопов. Пусть далее в соединении АХ содержится а р п атомов элемента X, участвующего в обмене. [17]
Можно показать, что при заданной дисперсии состояний о распределение по нормальному закону дает максимальное значение энтропии. [18]
Самопроизвольные процессы в изолированных системах могут протекать лишь в сторону возрастания энтропии, а равновесию соответствует максимальное значение энтропии. [19]
Вводя скорости и рассматривая неравновесные состояния, представляющие собой организмы, мы лишаемся такого надежного критерия, как максимальное значение энтропии, и должны попытаться найти другие основания для отбора состояний, являющихся устойчивыми. [20]
 |
Температуры стеклования и плавления ряда полимеров, области их применения. [21] |
При деформации такой системы суммарная величина статистической неупорядоченности уменьшается, поэтому система стремится возвратиться к состоянию, которому отвечает максимальное значение энтропии. [22]
Глубина самопроизвольных процессов определяется величиной энтропии каждого из тел, между которыми осуществляется какой-либо процесс, прекращающийся при достижении максимального значения энтропии, после чего система вступает в тепловое равновесное состояние, выйти из которого самопроизвольно не может. [23]
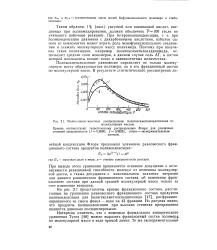 |
Молекулярно-массовое распределение полигексаметиленадипамида по. [24] |
При выводе этого уравнения принимается основное допущение о независимости реакционной способности молекул от величины молекулярной массы, а также допущения о максимальном значении энтропии для данного равновесного фракционного состава, об изменении фракционного состава при данной средней молекулярной массе только за счет изменения энтропии. [25]
Равновесию гетерогенных систем отвечает равенство химических потенциалов каждого компонента во всех фазах, а также минимальное значение одного из термодинамических потенциалов или максимальное значение энтропии всей системы при соответствующих условиях. Наиболее обычными условиями на практике являются постоянная температура и постоянное давление, поэтому мы будем оценивать равновесие гетерогенных систем по их изобарному потенциалу. [26]
Равновесию гетерогенных систем отвечает равенство химических потенциалов каждого компонента во всех фазах, а также минимальное значение изохорного или изобарного потенциалов или максимальное значение энтропии всей системы при определенных условиях. Если в систему входит хотя бы одна фаза, состав которой изменяется в процессе приближения к равновесию, то равновесное состояние фазы и всей системы характеризуется константой равновесия, например в системах, состоящих из индивидуальных веществ в конденсированном состоянии и газов. В системах, состоящих из индивидуальных веществ в конденсированном состоянии, в которых состав фаз в ходе процесса не изменяется, а процесс идет до полного исчезновения одного из исходных веществ ( например, полиморфные превращения веществ), понятие константы равновесия неприменимо. [27]
Равновесию гетерогенных систем отвечает равенство химических потенциалов каждого компонента во всех фазах, а также минимальное значение одного из термодинамических потенциалов или максимальное значение энтропии всей системы при соответствующих условиях. Наиболее обычными условиями на практике являются постоянная температура и постоянное давление, поэтому мы будем оценивать равновесие гетерогенных систем по их изобарному потенциалу. [28]
Принимая во внимание молекулярную природу рабочего вещества и флуктуации в нем внутренних параметров, можно отметить, что без установления равновесия в системе максимальное значение энтропии невозможно достигнуть. Флуктуации приводят систему к равновесию. Именно флуктуации в системах приводят к необходимости максимума энтропии при равновесии всякий раз, когда это условие не выполняется, то есть система выведена из равновесия. [29]
Принимая во внимание молекулярную природу рабочего вещества и флуктуации в нем внутренних параметров, можно отметить, что без установления равновесия в системе максимальное значение энтропии невозможно достигнуть. Флуктуации приводят систему к равновесию. Именно флуктуации в системах приводят к необходимости максимума энтропии при равновесии всякий раз, когда это условие не выполняется, то есть система выведена из равновесия. [30]
Страницы: 1 2 3 4