Рост - заряд - ядро
Cтраница 2
В пределах групп с ростом заряда ядра и накоплением электронных слоев ( сверху вниз) радиусы атомов растут - более быстро в А-группах и медленнее в В - и С-группах. [16]
Сверхтонкое расщепление увеличивается с ростом заряда ядра Z, а также с увеличением степени ионизации атома приблизительно пропорционально ZZa2, где Za - заряд атомного остатка. [17]
Константа экранирования для кайносимметриков при росте заряда ядра не имеет крутого хода кверху; эффективный ядерный заряд, следовательно, для них быстро увеличивается, а с ним и потенциалы ионизации, зависящие от глубины положения энергетического уровня. [18]
Изложенное показывает, что по мере роста заряда ядра происходит закономерная периодическая повторяемость сходных электронных структур элементов, а следовательно, и повторяемость их свойств, зависящих от строения электронной оболочки атомов. [19]
 |
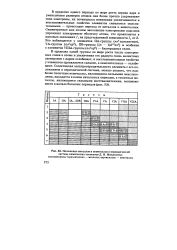
Зависимость значений электроотрицательности ЭО элементов ( черные кружки, первых потенциалов ионизации 1 ( светлые кружки и сродства к электрону ( - J - их атомов от зарядов ядер атомов ( Z. [20] |
В пределах одного периода по мере роста заряда ядра и уменьшения размеров атомов они более прочно удерживают свои электроны, их потенциалы ионизации увеличиваются и восстановительные свойства элементов сменяются окислительными - происходит переход от металлов к неметаллам. Симметричное или полное заполнение электронами подслоев упрочняет электронную оболочку атома, что проявляется в пиковых значениях 1 на представленной зависимости 1 от Z. Это наблюдается у элементов II А-группы ( п 2-заполнение), VA-группы ( ns2np3), II В-группы [ ( - l) d ns2 ] и особенно у элементов VIII А-группы ( ns rap6) - благородных газов. [21]
 |
Положение металлов и неметаллов в периодической. [22] |
В пределах одного периода по мере роста заряда ядра и уменьшения размеров атомов они более прочно удерживают свои электроны, их потенциалы ионизации увеличиваются и восстановительные свойства элементов сменяются окислительными - происходит переход от металлов к неметаллам. Симметричное или полное заполнение электронами подслоев упрочняет электронную оболочку атома, что проявляется в пиковых значениях 1г на представленной зависимости 1г от Z. Это наблюдается у элементов ПА-группы ( гав2 - заполнение), VA-группы ( ns2np3), ПВ-группы [ ( п - I) d10res2 ] и особенно у элементов VIIIA-группы ( ns2npe) - благородных газов. [23]
Изложенное показывает, что по мере роста заряда ядра происходит закономерная периодическая повторяемость сходных электронных структур, а следовательно, и повторяемость свойств элементов. [24]
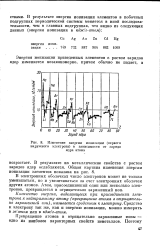 |
Изменение энергии ионизации ( первого. [25] |
В результате их металлические свойства с ростом зарядов ядер ослабляются. [26]
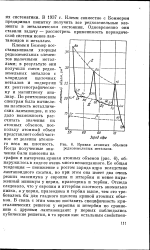 |
Кривая атомных объемов редкоземельных металлов. [27] |
Ее общая тенденция - понижение с ростом заряда ядра вследствие лантаноидного сжатия, но при этом она имеет два очень резких максимума у европия и иттербия и менее выраженный минимум у церия, празеодима и тербия. Отсюда следовало, что у европия и иттербия плотность аномально низка, а у церия, празеодима и тербия выше, чем это требовалось бы для гладкого наклона кривой атомных объемов. [28]
Период полураспада трансурановых элементов быстро уменьшается с ростом заряда ядра. [29]
Период полураспада трансурановых элементов быстро уменьшается с ростом заряда ядра. Для изотопа курчатовия 104Ки период полураспада составляет 70 - 0 1 с, для нильсбория losNs - 40 - 1 5 с, для 106-го элемента 0 9 - 0 007 с, а для 107-го элемента 0 002 с. Казалось бы, элементы с последующими атомными номерами должны иметь еще более короткие периоды полураспада. [30]
Страницы: 1 2 3 4