Рост - концентрация - электролит
Cтраница 1
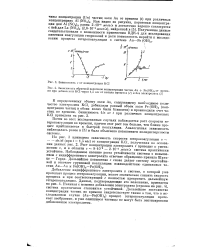 |
Зависимость v от концентрации КС1.| Зависимость обратной величины концентрации частиц Аи Fe ( OH3 от времени при добавлении КС1 через 1 5 час от начала процесса ( 1 и без электролита ( 2. [1] |
Рост концентрации электролита с приводит к уменьшению У, и в области с 8 - Ю 3 - 2 - Ю 2 молъ / л система практически устойчива. Наблюдаемое явление роста устойчивости системы с повышением с индифферентного электролита отвечает обращению правила Шуль-це - Гарди. [2]
С ростом концентрации электролита более сильное влияние на свойства раствора начинает оказывать процесс образования гидратов. В результате процесса гидратации изменяются размеры растворенных частиц, плотность их заряда, а также вязкость всего раствора в целом. С увеличением концентрации раствора электролита уменьшается среднее расстояние между противоположно заряженными ионами. При этом растет вероятность образования длительно существующих ионных пар, так называемых ионных двойников, основное отличие которых от молекул заключается в большей длине связи и наличии взаимодействующих с ионной парой молекул растворителя. [3]
С ростом концентрации электролитов, растворенных в воде, строение водных растворов постепенно меняется. Бек [25] измерял интенсивность рассеяния рентгеновских лучей в концентрированных водных растворах LiCl и LiBr ( например, 13 молей Lid на 1 л раствора) и показал, что строение концентрированных водных растворов подобно строению соответствующих кристаллогидратов. [4]
С ростом концентрации электролита подвижность ионов и его эквивалентная электропроводность снижается, особенно в области концентраций, применяемых в промышленных процессах электролиза. [5]
С ростом концентрации электролитов, растворенных в воде, строение водных растворов постепенно меняется. Бек [25] измерял интенсивность рассеяния рентгеновских лучей в концентрированных водных растворах LiCl и LiBr ( например, 13 молей LiCl на 1 л раствора) и показал, что строение концентрированных водных растворов подобно строению соответствующих кристаллогидратов. [6]
Однако, с ростом концентрации электролита в воде, проявляются также иные механизмы, влияющие на стабильность эмульсий. [7]
 |
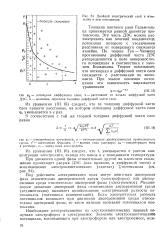
Схематическая зависимость константы А от хс при const ( a и а const ( б. [8] |
В этом случае с ростом концентрации электролита высота барьера практически не меняется, а, как показывают расчеты, лишь постепенно исчезает ближняя потенциальная яма. Поэтому при а const и А Ат л барьерный механизм коагуляции также невозможен. [9]
 |
Влияние электролита на содержание незамерзающей воды. [10] |
Снижение / С с ростом концентрации электролита обусловлено двумя факторами: прогрессирующим разрушением и утонь-шением гидратных ( незамерзающих) прослоек воды под влиянием электролита и уменьшением удельной поверхности дисперсной фазы латекса вследствие агрегации частиц. При концентрации NaCl более 0 5 кмоль / м3 латекс при замораживании коагулирует и эффект гидратации ( незамерзающей воды) исчезает. [11]
 |
Двойной электрический слой и изменение в нем потенциала. [12] |
Я, уменьшается с ростом концентрации электролита, заряда его ионов и с понижением температуры. [13]
Я, уменьшается с ростом концентрации электролита, заряда его ионов и с понижением температуры. [14]
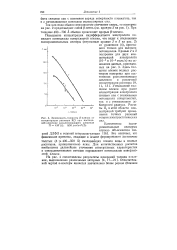 |
Зависимость толщины Р - пленок от концентрации раствора КС1 при постоянной величине расклинивающего давления П 430 ( / [ 1450 дин / см2 ( 2. [15] |
Страницы: 1 2 3 4 5