Рост - питтинг
Cтраница 2
Это, в свою очередь, означает, что рост питтинга в глубину замедляется по мере увеличения диаметра. [16]
Протекание этой реакции на отдельных участках приводит к процессу анодного роста питтингов. [17]
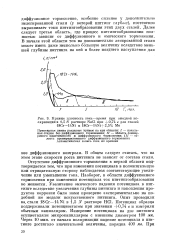 |
Кривые плотность тока-время при анодной поляризации в i 5N растворе NaCl при 0 74 в для сталей 18Сг - 14Ш и 18Cr - 14Ni 2 5 % Mo. [18] |
В общем следует считать, что на этом этапе скорости роста питтинга не зависят от состава стали. Отсутствие диффузионного торможения в первой области подтверждается тем, что при изменении потенциала в положительную или отрицательную сторону наблюдается соответствующее увеличение или уменьшение тока. Наоборот, в области диффузионного торможения при изменении потенциала ток питтингообразования не меняется. Увеличение омического падения потенциала в пит-тинге вследствие увеличения глубины питтинга и накопления продуктов коррозии было нами проверено экспериментально на подобной же модели искусственного питтинга. [19]
При анодном образовании питтинга следует различать три стадии: пробой пассивной пленки; первичный рост питтинга, где скорость роста определяется перенапряжением анодного процесса, а диффузионное торможение не имеет существенного значения; последующий рост питтинга, когда скорость растворения определяется диффузионными процессами. [20]
Следует различать три стадии развития питтинговой коррозии: 1) возникновение питтинга; 2) рост питтинга; 3) репассивацию. При некоторых условиях процесс питтинговой коррозии может стабилизироваться на второй стадии. Третья стадия не всегда реализуется, но практически является наиболее важной, так как в результате репассивации прекращается рост питтинга. [21]
Действительно, эксперименты, выполненные на сплавах Fe-Сг [75], показали, что увеличение скорости роста питтинга в этой области потенциалов обусловлено деформацией приповерхностных объемов металла и не связано ни с какими поверхностными эффектами или побочными реакциями. [22]
В основе механизма подавления питтингообразования лежит адсорбция ионов МоО2 - 4 на активных местах поверхности стали, подавляющих рост питтингов. Молибден в пассивных пленках находится в шестивалентном состоянии. Следовательно, сталь Х18Н12М2Т имеет значительно меньшую склонность к точечной коррозии в присутствии ионов хлора, чем другие марки сталей. [23]
Если роль окислителя сводить лишь к катодной деполяризации и исключить возможность пассивации металла внутри питтингов, то закономерности роста питтингов трудно объяснить. Казалось бы, что скорость проникновения коррозии в глубь металла должна с увеличением концентрации окислителя непрерывно расти вследствие ускорения катодного процесса. Между тем результаты экспериментов показывают, что увеличение окислительной способности раствора сверх определенной величины уменьшает не только число питтингов, но и среднюю их глубину. [24]
В области питтинговой коррозии при отсутствии диффузионного торможения как в кислых, так и нейтральных средах наблюдается линейная зависимость логарифма плотности анодного тока роста питтинга от потенциала для всех исследуемых сталей, что свидетельствует об электрохимической природе питтинговой коррозии. Высказано предположение, что анодное растворение при этом идет не путем непосредственного образования ионов металла низшей валентности, а через промежуточный процесс образования окисной пленки и последующего ее химического растворения. [25]
Аналогичные исследования кинетики роста питтинга были проведены на другой модели искусственного питтинга без наложения внешней анодной поляризации, более приближающейся к естественным условиям образования и роста питтинга. [26]
По адсорбционному механизму локальная депассивация металла хлор-ионами происходит вследствие адсорбционного вытеснения ими кислорода на участках с ослабленной связью кислорода и металла. Начальной стадии роста питтинга соответствует возможное растворение структурных элементов поверхности, дающих менее совершенную пассивацию. На этой стадии отсутствует характерная округлая ( полусферическая) форма питтинга и заметные концентрационные изменения электролита в первичном питтинге. [27]
Снижение средней скорости роста питтинга ( определенной из глубин образования питтинга за ЗОмин. [28]
Описанное выше исследование анодного процесса на модели искусственного питтинга относится, как уже указывалось, к процессам, происходящим в начальной стадии развития питтинга, когда глубина его незначительна и торможение анодного процесса затруднениями диффузионного и омического порядка является несущественным. Очевидно, с увеличением времени роста питтинга ( главным образом вследствие его развития в глубину) анодные процессы в питтингах все в большей степени начнут тормозиться диффузионными процессами и возросшим омическим сопротивлением продуктов коррозии в питтинге. [29]
Измерение распределения питтингов по размерам после отдельных длительных испытаний показывает, что размеры питтингов не одинаковы; обычно только небольшая часть их имеет значительные размеры, а большая часть - малые размеры. Это может быть обусловлено или разной скоростью роста питтингов, или прекращением роста ( репассивацией) значительного числа питтингов в начальный период коррозии. При росте питтинга в нем происходит накопление С1 - и под-кисление раствора. Это приводит к изменению пассива-ционных характеристик металла в питтинге ( сдвигу потенциала полной пассивации Епи в положительную сторону - точка С и потенциала питтингообразованияв отрицательную сторону - точка D), которое уменьшает область пассивного состояния. Однако, если область пассивного состояния ( C D) все же остается, то репассп-вация питтинга, возможна. С углублением питтинга возрастает омическое падение потенциала между дном питтинга и поверхностью металла и происходит смещение потенциала в питтинге в отрицательную сторону на величину IR. [30]
Страницы: 1 2 3 4