Рост - скорость - коррозия
Cтраница 1
Рост скорости коррозии в интервале концентраций 0 - 5 % связан с увеличением проводимости раствора и стимулирующим действием ионов хлора, являющихся эффективными активаторами. Замедление роста скорости коррозионных проявлений и их торможение при большем солесодержании определяется снижением растворимости H2S и уменьшением агрессивности электролита. [2]
Рост скорости коррозии внутренней поверхности нефтепромысловых резервуаров обусловлен не только активностью коррозионной среды и наличием неоднородности в структуре металла, но и действующими растягивающими напряжениями. [3]
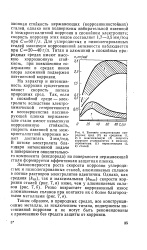 |
Влияние концентрации природных сред ( С на среднюю ( 1. [4] |
Закономерности роста скорости коррозии углеродистых и низколегированных сталей, алюминиевых сплавов в потоке растворов электролитов идентичны. [5]
В техническом магнии росту скорости коррозии более всего способствуют примеси железа, никеля и меди, причем железо влияет в наибольшей степени. Если в металле присутствуют марганец и цинк, то допустимый предел поднимается до более высоких значений. Помимо этого, действие марганца, видимо, связано с образованием нерастворимого интерметаллического соединения, в состав которого входит железо. Это соединение тяжелее магния и так же, как и в случае алюминия ( разд. [6]
С повышением температуры наблюдается рост скорости коррозии, затем замедление ее и последующее уменьшение. Максимум скорости коррозии с увеличением давления СО2 смещается в сторону более высоких температур. С увеличением скорости газожидкостного потока от 2 до 8 - 10 м / с скорость углекислотной коррозии возрастает в 1 5 - 2 раза, затем несколько замедляется и при скоростях потока 10 - 12 м / с скорость коррозии резко возрастает от действия коррозионно-эрозионного фактора, особенно в местах завихрений и турбулизации потока. С уменьшением парциального давления в скважинах максимум величины коррозии и область эрозионной коррозии перемещаются в сторону больших скоростей потока. Повышение коррозионного действия при увеличении скорости потока объясняются увеличением притока к катодным участкам молекул СО2 и возможностью их участия в катодном процессе. Известно, что при одной и той же величине рН коррозия в углекислотной водной среде протекает более интенсивно, чем в растворе сильных кислот. [7]
В данной среде причиной роста скорости коррозии, несомненно, служит повышение концентрации углерода. Таким образом, углерод в железоуглеродистых сплавах является компонентом, ускоряющим коррозионное разрушение в кислых средах. В нейтральных растворах углерод не оказывает ускоряющего влияния на скорость коррозии, а в некоторых окислительных средах он действует благоприятно, уменьшая скорость коррозии. [8]
Повышение температуры обычно приводит к росту скорости коррозии. При повышении температуры на 10 скорость обычно удваивается. Но во многих случаях коррозия достигает максимума около 80 С. При дальнейшем повышении температуры она часто снижается в результате уменьшения растворимости кислорода. [9]
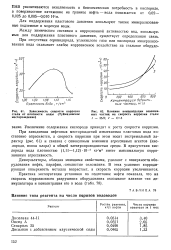 |
Зависимость скорости коррозии стали от плотности воды ( Туймазинское месторождение.| Влияние концентрации взвешенных частиц на скорость коррозии стали. [10] |
Увеличение содержания кислорода приводит к росту скорости коррозии. [11]
Дальнейшее увемченив концентрации аммиака приводило к росту скорости коррозии чугуна, что связано, по-видимому, с повышением растворимости пленки гидроокиси железа ори высоких значениях рН и температурах. [12]
 |
Образец меди после испытаний в хладоне 11 при 150 С ( Х2.| Поверхность латуни после испытаний в хладоне 11 при температуре 150 С ( Х800. [13] |
Как и в случае хладона 11, рост скорости коррозии при 200 - 250 С обусловлен разложением хладона 12 на поверхности автоклава. Продукты разложения взаимодействуют с образцами металлов, образуя хлориды железа и меди. [14]
Увеличение минерализации электролита в двухфазной системе ведет к росту скорости коррозии углеродистой стали. Повышение скорости коррозии в присутствии сульфата железа может быть объяснено своеобразным влиянием двухвалентных ионов железа, которые при небольшом изменении рН электролита в тонком слое способствуют более быстрому образованию на поверхности металла осадда сульфида железа, стимулирующего коррозию. [15]
Страницы: 1 2 3 4
