Рост - скорость - коррозия
Cтраница 3
Коррозия углеродистых сталей, меди и медных сплавов при низких температурах обусловлена гидролизом раона под иллинием содержанием в йен влаги. Рост скорости коррозии этих металлов при 2СЮ - 250ССобусловлен разлокениен fпеона на поверхности автоклава. Продухтн разложения взаимодействуют с огЗрчзцами металлов с обртоовпнием хлоридов железа и меди ( Ги у. Teunepirypax увеличивается с ростом длительности ио-пьганий, так как вэтом случае возрастает степень термического разложения реона ( табл. 1), а образующиеся порошкообразные продукты коррозии меди / однохлористая издь / не об-ладаиг заадтнши свойствами. Угдпродистые стали более стойки при инеокию температурах, т.к. на поверхности ойразуот - CR тружяоонт яе ы9 защитные пленки. [31]
Коэффициент деформационного упрочнения m отражает влияние на МХЭ предельной степени пластической деформации. Параметр Кст характеризует интенсивность роста скорости коррозии с увеличением пластичесой деформации. [32]
Видно, что скорость локальный коррозии при расслоенном режиме течения в десятки раз выше скорости равномерной коррозии при дисперсно-кольцевом режиме. Повышение концентрации сероводорода в обоих случаях приводит к росту скорости коррозии внутренней поверхности газопровода. [33]
Видно, что скорость локальный коррозии при расслоенном режиме течения в десятки раз выше скорости равномерной коррозии при дисперсно-кольцевом режиме. Повышение концентрации сероводорода в обоих случаях приводит к росту скорости коррозии внутренней повеохности газопровода. [34]
По-видимому, на ход поляризационной кривой в условиях образования на металле объемистого осадка сульфида железа определенное влияние может оказать изменение истинной поверхности электрода. Это также должно вести к повышению кривой катодной поляризации и к росту скорости коррозии, так как известно, что с увеличением истинной поверхности электрода понижается перенапряжение выделения водорода. [35]
 |
Фотография элемента трубы нефтепровода СУН Султанаево - НСП Красный холм с отложившимся солевым осадком ( а и с удаленным осадком ( б, под которым виден след питтинговой коррозии. [36] |
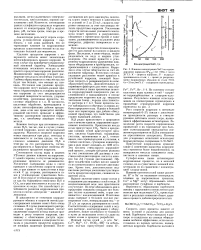
При этом содержание H2S за весь анализируемый период в попутно-добываемой воде изменилось незначительно. Кривые на рис. 3, таким образом, свидетельствуют о прямой связи роста скорости коррозии от содержания FeS в осадке. [37]
Определенный интерес при этом представляет оценка влияния концентрации сероводорода на коррозию углеродистой стали. Большинство исследователей пришло к мнению, что увеличение концентрации сероводорода в растворе способствует росту скорости коррозии до известного предела, после чего скорость коррозии стабилизируется. Была изучена коррозия железа в присутствии сероводорода в среде минерализованной воды и легких углеводородов. [38]
Для количественной оценки роли сульфидов железа в усилении коррозии в [128] изучено изменение стационарного потенциала коррозии стального образца в контакте с отложениями сульфидов. Установлен сдвиг потенциала металла образца в положительную сторону на 80 - 120 мВ и рост скорости коррозии в 15 - 17 раз. [39]
В зависимости от геометрии корродирующего объекта и скорости потока рассматриваемое влияние может быть очень сложным. В случае равномерного распределения среды ( турбулентный поток) увеличение скорости потока вначале приводит к росту скорости коррозии, связанному с облегчением доступа агрессивных составляющих к поверхности металла и удалением продуктов коррозии, не носящих защитных функций. [41]
Этот кислород, по мнению авторов, частично входит в кристаллическую решетку РЬО2 в виде сверх-стехиометрических атомов и диффундирует через слой окисла к поверхности металла, окисляя его. Авторами допускается также возможность окисления свинца под слоем РЬО2 в результате проникновения электролита между кристаллами или агломератами двуокиси. Рост скорости коррозии при увеличении температуры и времени поляризации, установленный в указанных работах, объясняется влиянием этих факторов на скорость диффузии кислорода. [42]
По ходу экспериментальной кривой 1 на рисунке 4.6 видно, что конденсация паров солей щелочных металлов на образце прекратится в указанном интервале температур. Получить отложения при такой высокой температуре в чистом виде не удается, так как после 500 резко возрастает скорость коррозии, и отделить щелочьсодержащий слой от окалины, покрывающей образец, трудно. С ростом скорости коррозии уменьшается скорость конденсации щелочей на поверхности в результате того, что температура окисленной и покрытой отложениями поверхности со стороны газа превышает температуру металла под этим слоем, измеряемую термопарой. Когда температура слоя достигает температуры газов, конденсация вообще прекращается. Поэтому с ростом температуры поверхности и увеличением длительности опыта средняя скорость роста отложений падает. [43]
Помимо рН и РС02 другим важным фактором, определяющим скорость и механизм углекислотной коррозии, является температура. В отличие от кислотной коррозии зависимость скорости углекислотной коррозии от температуры неоднозначна. С повышением температуры рост скорости коррозии наблюдается лишь до 40 - 60 С, а затем происходит ее торможение, что объяснено сменой механизма. При температуре 25 - 40 С образуется пористая, проницаемая для деполяризатора оксид-гидроксидная пленка, иногда с вкраплениями карбоната железа. При температуре 60 С пленка / отложения продуктов коррозии становится более плотной, что повышает ее защитные свойства. Изменяется состав продуктов коррозии - вместо оксид-гидроксидной формируются карбонатно-гидрокарбо-натные и чисто карбонатные пленки / отложения ( с вкраплениями цементита при Т 100 С), при этом характер лимитирующей стадии меняется. [44]
Помимо рН и РСО2 другим важным фактором, определяющим скорость и механизм углекислотной коррозии, является температура. В отличие от кислотной коррозии зависимость скорости углекислотной коррозии от температуры неоднозначна. С повышением температуры рост скорости коррозии наблюдается лишь до 40 - 60 С, а затем происходит ее торможение, что объяснено сменой механизма. При температуре 25 - 40 С образуется пористая, проницаемая для деполяризатора оксид-гидроксидная пленка, иногда с вкраплениями карбоната железа. При температуре 60 С пленка / отложения продуктов коррозии становится более плотной, что повышает ее защитные свойства. Изменяется состав продуктов коррозии - вместо оксид-гидроксидной формируются карбонатно-гидрокарбо-натные и чисто карбонатные пленки / отложения ( с вкраплениями цементита при Т 100 С), при этом характер лимитирующей стадии меняется. [45]
Страницы: 1 2 3 4