Рост - теплоемкость
Cтраница 1
Рост теплоемкости при увеличении температуры газа происходит сравнительно медленно. С), вполне возможно и целесообразно принять значение теплоемкости постоянным. При значительном изменении температуры газа в процессах, происходящих в двигателях внутреннего сгорания и газовых турбинах, а также при охлаждении продуктов сгорания топлива в газоходах котла необходимо считать теплоемкость зависящей от температуры. [1]
 |
Параметры аппроксимационных уравнений [ 46, с. 98 - 104 ]. [2] |
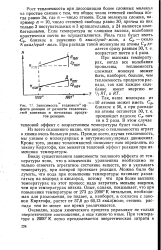
Рост теплоемкости при температурах выше 2200 С стабилизируется. Однако выше температуры 3200 С снова происходит резкий ее рост, экспоненциально связанный с температурой. Величина энергии активации, равная 7 7 эВ, близка к теплоте испарения атомов углерода. Поэтому возрастание удельной теплоемкости при высоких температурах может быть связано с образованием дефектов кристаллической решетки ( вакансий) вследствие испарения графита. [3]
 |
Зависимость теплового эффекта реакции от разности теплоемкостей конечных и начальных продуктов реакции. [4] |
Рост теплоемкости при диссоциации более сложных молекул на простые связан с тем, что общее число степеней свободы всегда равно 3, где п - число атомов. Если молекула сложна, например п 10, число степеней свободы равно 30, причем из них только 3 поступательных и 3 вращательных, а 24 являются колебательными. Если температура не слишком высока, колебания практически почти не осуществляются. Моль газа будет иметь - Cv, близкое к значению 6 ккал / град моль, а Ср - около 8 ккал / град моль. [5]
Рост теплоемкости С при приближении к J происходит по ло-гарифмич. [7]
Рост теплоемкости С при приближении к 7 происходит по ло-гарнфмич. [9]
К рост теплоемкости Cs быстро замедляется. Около 150 К имеется еще одна точка перегиба, но для более простых и низкоплавких по сравнению с нафталином твердых веществ второй перегиб часто не наблюдается. Кривая непрерывна до точки плавления ( тройной темпера турной точки 7 р) и не имеет переломов и каких-либо разрывов. Примерно две трети изученных органических кристаллов характеризуются кривыми теплоемкости, которым свойственны все эти особенности, исключая в некоторых случаях высокотемпературную точку перегиба. [10]
Отсюда понятен рост теплоемкости в области предплавления, так как только часть введенного тепла идет на нагревание вещества, а большая часть расходуется на плавление основного компонента. Если учесть, что теплота плавления на 3 Ч - 4 порядка больше теплоемкости, то становится ясной причина высокой чувствительности определения содержания примеси из определения теплоемкости в области предплавления. [11]
Переход сопровождается ростом теплоемкости. [12]
Чтобы экспериментально доказать рост теплоемкости газа при увеличении его объема, Деларош и Берар [10] измерили ( 1813 г.) теплоемкость ряда газов при постоянном давлении. [13]
Другой причиной, вызывающей рост теплоемкости многоатомных газов с увеличением температуры, является диссоциация молекул. При увеличении температуры газа происходит частичный распад сложных молекул на более простые. Этот процесс называется термической диссоциацией. Затрата энергии на диссоциацию приводит к увеличению теплоемкости газов. [14]
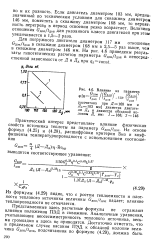 |
Влияние на параметр. [15] |
Страницы: 1 2 3

