Рост - число - атом
Cтраница 3
Соли первичных аминов плохо растворимы в органических растворителях - их растворимость увеличивается с ростом числа атомов углерода в алкильной цепи и - по мере повышения значения относительной диэлектрической проницаемости среды. Соли вторичных и третичных аминов - более растворимы в органических растворителях. Растворимость солей четвертичных аммониевых оснований также зависит от числа атомов углерода в молекуле. Бели оно меньше 15, то эти соли более растворимы в воде, чем в органических растворителях; если же оно превышает 24, то справедливо обратное соотношение. В некоторых практических применениях используется смесь, содержащая амины различных типов. [31]
Относительная вероятность образования осколочных ионов, отвечающих удалению электрона с а-орбиталей, увеличивается с ростом числа атомов углерода в алкильной группе. [32]
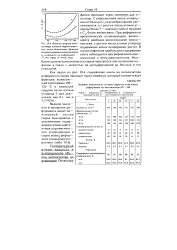 |
Влияние средних тем - неНТЭМИ, С ростом ЧИСЛЗ ЗТОМОВ углерода. [33] |
С уменьшением числа углеродных атомов до С5 коксообразование уве - личивается, а с ростом числа атомов углерода более 7 - вначале слабо и начиная с С) 0 более интенсивно. [34]
Понижение температуры размягчения кварцевого стекла при добавлении к нему соды вызывается нарушениями кремние-кисло-родной решетки вследствие роста числа атомов кислорода, связанных лишь с одним атомом кремния. Вследствие разрушения все большего количества этих связей структура становится менее жестко связанной в трех измерениях. Благодаря отсутствию структурных повторений в стекле в нем нет и пары точно одинаковых точек. В ем имеются точки с широко меняющейся степенью ослабления, в которых при непрерывном изменении температуры может иметь место текучесть или разрушение. [35]
При переходе к сфероидальной форме фуллерена ( при Сх С60) мера устойчивости симметрии к росту числа атомов углерода снижается, но самоподобная связь между мерой устойчивости симметрии и кодом обратной связи сохраняется. [36]
Он слабо растворим в парафиновых углеводородах типа пентан, гексан и декан, причем с ростом числа атомов углерода растворимость в алканах возрастает. [37]
Интересно, что в растворах, содержащих не более 60 % метанола, разряд тетраалкиламмониевых катионов с ростом числа атомов углерода в алкиле выше четырех вновь облегчается, что, по-видимому, обусловлено [159] возможностью деформации длинных алкильных цепей, в результате чего реакционный центр ( положительно заряженный атом азота) приближается к поверхности электрода. При замене нормальных алкильных заместителей на их изомеры изостроения разряд тетразаыещенных катионов аммония затрудняется, что связано, по-видимому, с меньшей деформируемостью алкильных цепей изостроения. Однако в 90 % - ном мсганоле почти нет различия в легкости разряда тетразаме-щенных аммониев с алкилами нормального и изостроепвя [158], а также не наблюдается облегчения разряда при увеличении длины цепи, даже при переходе к тетра-н-октшшроизводному, поэтому можно предположить, что в среде с высоким содержанием органического растворителя деформация алкильных заместителей тетраалкиламмониевых ионов на поверхности электрода затруднена. [38]
Можно предположить, что и для других гомологических рядов должно наблюдаться аналогичное изменение величин отношения объемов удерживания с ростом числа атомов углерода. [39]
В отличие от адсорбции на гидроксилированной поверхности си-ликагеля ( см. рис. 12.1), удерживание в этом случае с ростом числа атомов углерода в молекуле возрастает как в ряду поли-метилбензолов, так и в ряду моно-н-алкилбензолов. Поскольку при использовании силанизированного силикагеля и элюента изопропанола и воды удерживание преимущественно определяется неспецифическим межмолекулярным взаимодействием вещество - адсорбент и специфическим межмолекулярным взаимодействием вещество - элюент, моно-н-алкилбензолы удерживаются сильнее соответствующих полиметилбензолов с тем же числом атомов углерода в молекуле. [41]
Как видно, для атомных стабилизаторов ( инертные газы) эффективность стабилизации растет с увеличением атомной массы, для молекулярных - с ростом числа атомов в молекуле. & c2H5i 38, но обшая картина остается типичной. [42]
Как видно, для атомных стабилизаторов ( инертные газы) эффективность стабилизации растет с увеличением атомной массы, для молекулярных - с ростом числа атомов в молекуле. & c2H5i 38, но общая картина остается типичной. [43]
Как видно, для атомных стабилизаторов ( инертные газы) эффективность стабилизации растет с увеличением атомной массы, для молекулярных - с ростом числа атомов в молекуле. Правда, при более детальном рассмотрении наблюдается и некоторая специфичность действия, например, AC2H5ci 46 3, & с2н5вг14, 2 & с2н51 38, но общая картина остается типичной. [44]
Страницы: 1 2 3 4 5