Рутенат
Cтраница 1
Рутенат образуется при поглощении Ru04 раствором щелочи или при экстракции Rn04 щелочью из раствора в четырех-хлористом углероде. Перрутенат образуется в щелочной среде в присутствии гипохлорита или периодата. [1]
Время стояния раствора рутената с соляной кислотой также влияет на выход комплекса. [2]
Маршал и Рикард [605] считали раствор рутената довольно неустойчивым. По данным Андерсона и др., неустойчивость свойственна только свежим растворам и объясняется использованием новой стеклянной посуды. При работе с посудой, в которой в течение нескольких дней выдерживался щелочной раствор рутената, устойчивость окрашенного комплекса возрастает от 30 мин до нескольких дней. [3]
При добавлении спирта в щелочной раствор рутената, полученного при отгонке четырехокиси рутения в 6 N NaOH, выделяется черный осадок. Если в растворе находится менее 1 мг рутения, то вначале появляется зеленое окрашивание, а через несколько минут выпадает осадок. Даже 50 мг осмия не мешают открытию рутения. [4]
Кислые растворы перрутената калия неустойчивы и разлагаются с образованием оранжевого рутената и выделением кислорода. [5]
Процесс получения катализаторов сводился к следующему: рутений превращался в рутенат сплавлением со щелочью в присутствии окислителя. [6]
Ларсен и Росс [598] сообщили, что им не удалось определить рутений по окраске рутената, полученного при поглощении че-тырехокиси рутения 9 М раствором едкого натра, так как при этом иногда образуется нерастворимая двуокись рутения. [7]
 |
Потенциалы кислородных соединений рутения в щелочных растворах.| Спектры Ruvl ( /, Ruvl и Ruvn ( 2 и Ruvu ( 3 в 1 М растворе NaOH. [8] |
При поглощении тетраокси-да рутения щелочью сначала образуется зеленый перрутенат, который затем восстанавливается до красного рутената. Рутенат и перрутенат значительно более устойчивы в щелочных растворах, чем в кислых. При дистилляции RuC4 из растворов НС1 образуются хлоридные комплексы рутения. Показано [3], что устойчивые растворы перрутената получаются только при поглощении тетраоксида рутения раствором 1 М NaOH, содержащим гипохлорит. При более высоких концентрациях щелочи ( 6 М) перрутенат быстро восстанавливается до рутената даже в присутствии гипохлорита. В работе [4] устойчивые растворы перрутената получены поглощением тетраоксида рутения 0 5 - 1 0 М раствором Na2COa, содержащим гипохлорит. [9]
В мерную колбу вместимостью 25 мл вливают анализируемый раствор с содержанием до 0 15 мг рутения ( в форме рутената), 3 М NaOH до концентрации его 0 5 - 1 М в конечном объеме, 5 мл 1 М маннита, воду до метки. Приготовленный раствор выдерживают в кипящей водяной бане 6 мин, охлаждают. Измеряют ОП при 350 нм относительно раствора реагентов. [10]
 |
Потенциалы кислородных соединений рутения в щелочных растворах.| Спектры Ruvl ( /, Ruvl и Ruvn ( 2 и Ruvu ( 3 в 1 М растворе NaOH. [11] |
При поглощении тетраокси-да рутения щелочью сначала образуется зеленый перрутенат, который затем восстанавливается до красного рутената. Рутенат и перрутенат значительно более устойчивы в щелочных растворах, чем в кислых. При дистилляции RuC4 из растворов НС1 образуются хлоридные комплексы рутения. Показано [3], что устойчивые растворы перрутената получаются только при поглощении тетраоксида рутения раствором 1 М NaOH, содержащим гипохлорит. При более высоких концентрациях щелочи ( 6 М) перрутенат быстро восстанавливается до рутената даже в присутствии гипохлорита. В работе [4] устойчивые растворы перрутената получены поглощением тетраоксида рутения 0 5 - 1 0 М раствором Na2COa, содержащим гипохлорит. [12]
К порошкообразному рутению приливают 4 N раствор NaOH, смесь осторожно доводят до кипения, внося небольшими порциями персульфат калия. При этом получается темно-красный раствор рутената, довольно устойчивый, если его хранить в холодильнике, с избытком персульфата. [13]
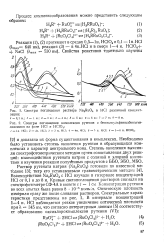 |
Спектры поглощения комплексов рутения с бензолсульфонилбензами-яоксимом на фоне НС1 и НС. 04. [14] |
Необходимо было установить степень окисления рутения в образующихся комплексах и характер центрального иона. Степень окисления выясняли спектрофотометрическим методом путем сопоставления двух реакций: взаимодействия рутената натрия с соляной и хлорной кислотами и изучения реакции полученных продуктов с ББО, ЭБО, МБО. [15]
Страницы: 1 2