Рутенат
Cтраница 2
Остаток, состоящий из родня, иридия и рутения, хлорируют на слое хлорида натрия, сплавляют с едким натром и перекисью натрия или чередуют эти операции. Первая из этих операций дает растворимый в воде хло-рородиг, а вторая приводит к получению водорастворимого рутената и соединения иридия, растворимого в соляной кислоте. Из полученных таким путем растворов родий осаждается в виде гексапитритородита аммония, а иридий - в виде хлороиридата ( 1У) аммония. Для выделения рутения четырехокись рутения дистиллируют в токе хлора и поглощают ее раствором разбавленном соляной кислоты. Из получаемого раствора путем добавления хлорида аммония осаждают - рутений. [16]
 |
Прибор для улавливания четы-рехокиси рутения. [17] |
Вводная и выводная трубки снабжены стеклянными пробками. Все шлифы должны быть выполнены очень тщательно. При начале отгонки пропускают умеренный ток хлора в холодный раствор рутената. Когда хлор перестает поглощаться, начинают нагревать водяную баню, увеличивая скорость тока хлора - Операцию можно считать законченной, если содержимое перегонной колбы станет почти бесцветным. [18]
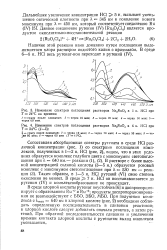 |
Изменение спектров поглощения растворов Na2RuO4 в 1 н. НС1 при. [19] |
В среде хлорной кислоты рутенат неустойчив [6] и диспропорцио-нирует с образованием Ru 7 и Ru 5; продукты диспропорционирова-ния не взаимодействуют с ББО, ЭБО, МБО. При получении комплекса с Ятах 640 нм в хлорной кислоте ( рис. 2) необходимо соблюдать определенную последовательность в сливании реактивов; к хлорной кислоте следует добавлять сначала реактив, а затем рутений. При обратной последовательности сливания и увеличении времени контакта хлорной кислоты с рутенатом выход комплекса уменьшается. [20]
Маршал и Рикард [605] считали раствор рутената довольно неустойчивым. По данным Андерсона и др., неустойчивость свойственна только свежим растворам и объясняется использованием новой стеклянной посуды. При работе с посудой, в которой в течение нескольких дней выдерживался щелочной раствор рутената, устойчивость окрашенного комплекса возрастает от 30 мин до нескольких дней. [21]
Тонкоизмельченную навеску почвы помещают в никелевый тигель, добавляют растворы, содержащие носители Sr, Cs, Ce, Ru, и выпаривают содержимое тигля досуха под лампой для выпаривания. Затем в тигель добавляют щелочную смесь КОН-КМОз-К2СОз ( в соотношении 2: 1: 1) в 5 - 10-кратном количестве от массы образца почвы и прокаливают материал в муфеле при 500 С в течение 2 ч, через каждые 15 - 20 мин вращая тигель. При сплавлении кремневая кислота переходит в растворимую форму, а рутений окисляется с образованием растворимого рутената. Сплав охлаждают и выщелачивают двукратно 10 - 15 мл горячей дистиллированной воды. При этом Cs и Ru растворяются, a Sr, Се и другие изотопы остаются в плаве в виде нерастворимых карбонатов и гидроокисей. Плав после охлаждения обрабатывают соляной кислотой. [22]
Исследованы два носителя: оксид бария и оксид магния. Они показали различные, но связанные эффекты. В случае с оксидом бария [18] ( приоритет сотрудников фирмы Форда) рутений и оксид бария взаимодействуют в окислительных условиях с образованием рутената BaRuOs. При восстановительных условиях рутений возвращается в восстановленное состояние и участвует в каталитической реакции. [23]
Стил и йо [587] применяли этот реактив, образующий растворимый в воде, устойчивый красный комплекс состава R2RuO4 с максимумом светопоглощения при 530 ммк, для определения 0 5 - 14 мкг / мл рутения. Окраска при комнатной температуре развивается мгновенно. Рекомендуемые кислотность и количество реагента можно не соблюдать слишком строго. Кислотность поглощающего раствора выбирают с таким расчетом, чтобы ион рутената не разложился. Определению мешают многие примеси, поэтому необходима отгонка рутения. Осмий также взаимодействует с этим реагентом, образуя комплексное соединение, пригодное для спектрофотометри-ческого определения. Поэтому растворы предварительно кипятят с азотной кислотой для удаления осмия. [24]
Эти соединения предварительно должны быть разрушены и рутений отогнан в виде четырехокиси из смеси серной и хлорной кислот. Нитраты или нитриты разрушают при повторном выпаривании с концентрированной соляной кислотой с последующим упариванием с серной кислотой до появления паров последней. Рутенат: ы ( У1) и перрутенаты ( УП) сначала переводят в RuO2 - H2O, который затем растворяют в соляной кислоте. Дефорд рекомендует применять иодид для восстановления окислителей ( даже четырехвалентного рутения), которые в противном случае будут давать помутнение за счет окисления тиомочевины. Освобождающийся иод следует удалить кипячением, которое должно продолжаться не дольше, чем это необходимо. [25]
Исследованы два носителя: оксид бария и оксид магния. Они показали различные, но связанные эффекты. В случае с оксидом бария [18] ( приоритет сотрудников фирмы Форда) рутений и оксид бария взаимодействуют в окислительных условиях с образованием рутената BaRuOs. При восстановительных условиях рутений возвращается в восстановленное состояние и участвует в каталитической реакции. Проблемой применения этих веществ является устранение их недолговечности, отчасти из-за периодических превращений между рутенатом и металлическим рутением. Использование оксида магния ликвидирует данную проблему, так как он не образует рутенат в основной массе. [26]
Исследованы два носителя: оксид бария и оксид магния. Они показали различные, но связанные эффекты. В случае с оксидом бария [18] ( приоритет сотрудников фирмы Форда) рутений и оксид бария взаимодействуют в окислительных условиях с образованием рутената BaRuOs. При восстановительных условиях рутений возвращается в восстановленное состояние и участвует в каталитической реакции. Проблемой применения этих веществ является устранение их недолговечности, отчасти из-за периодических превращений между рутенатом и металлическим рутением. Использование оксида магния ликвидирует данную проблему, так как он не образует рутенат в основной массе. [27]
Страницы: 1 2