Найденное значение - энергия - активация
Cтраница 1
Найденное значение энергии активации позволяет сделать ряд предположений о природе взаимодействующего с границей дефекта. Этот дефект должен быть значительно более подвижным, чем протонная вакансия, которая, как показывают эксперименты по измерению электропроводности в этих кристаллах, имеет энергию активации своего движения 0 54 эВ [246-248] и, следовательно, практически неподвижна в интересующей нас области температур 100 К. В тоже время он должен быть менее подвижным, чем дефекты Такаги, и, значит, вносимое таким дефектом искажение кристаллической решетки должно быть промежуточным по сравнению с искажениями, вносимыми указанными структурными нарушениями. Этим требованиям удовлетворяет замеченный в ЭПР спектрах [249] дефект вида ( Н2РО4) 2, который формируется путем захвата дырки обедненной протонами РО3 - структурной единицей кристалла. [1]
Найденное значение энергии активации довольно близко к величине энергии активации процесса гомополимеризации хлористого винила 3, что можно рассматривать как дополнительное доказательство прохождения реакции в кинетической области. [2]
Найденные значения энергии активации возрастают с увеличением степени отверждения в связи с ростом влияния на процесс полимеризации диффузионных факторов. Продукты полимеризации имеют сложный состав и включают жидкий слой, идентифицированный как не вступившие в реакцию мономеры, а также полимеризат с содержанием в зависимости от природы мономеров и условий полимеризации 69.2 - 90.3 % гель-фракции. Применение увеличенного количества радикальных инициаторов и окислительно-восстановительных систем позволяет увеличить глубину отверждения, исключить наличие жидкой фазы незаполимеризовавшихся мономеров и получить гомополимеры с более высоким уровнем физико-механических свойств, чем при полимеризации моно-метакриловых производных кислот фосфора вследствие образования густосетчатой структуры. Полимеры ди-р-метакрилоиловых производных фосфоновых и фосфорных кислот имеют теплостойкость по Вика 130 - 145 С, низкое водопоглощение ( 1.20 - 1.25 % за 30 суток), температура начала их термоокислительной деструкции составляет 160 - 165 С. [3]
Найденное значение энергии активации находится в согласии с имеющимися в настоящее время данными о предельных углеводородах. Таким образом, мы видим, что произведенные количественные оценки выводов теории говорят в ее пользу. [4]
Найденные значения энергии активации и предэкспоненты указывают, что эта константа является эффективной величиной, значение которой больше истинной константы скорости распада гидроперекиси на радикалы. Поскольку истинная константа скорости распада гидроперекиси на радикалы в водной фазе должна иметь значение К 2 7 108 е - 22300 / кт Сек-1, то и истинная величина а должна быть еще меньше. [5]
Найденные значения энергии активации процесса радикальной полимеризации в присутствии ДАК составляют в зависимости от строения полимеризуемых мономеров 60 - 110 кДж / моль. Выявлено, что, несмотря на удаленность фосфорсодержащей группы от двойной связи, ее строение оказывает влияние на скорость полимеризации. [6]
Поскольку найденное значение энергии активации образования свободного серебра во втором созревании оказалось очень близким к той же величине, полученной для реакции восстановления в гомогенной системе AgN03 - желатина, то нужно думать, что установленная температурная зависимость относится не к адсорбционному процессу, а к реакции распада образовавшихся адсорбционных комплексов. [7]
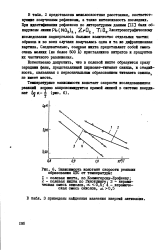 |
Зависимость констант скорости реакции образования ЦТС от температуры. [8] |
В табл. 3 приведены найденные значения энергий активации. [9]
Следует отметить, что найденные значения энергии активации значительно ниже известных литературных данных, а также значения энергии активации для объемной пластической деформации, определенного при тех же условиях деформирования. Значение энергии активации для пластического течения внутренних объемных слоев материала определялось известным в литературе [458, 459] графо-аналитическим способом по температурно-скоростному изменению верхнего предела текучести. [11]
Диффузионный контроль процесса коррозии титана в пассивном состоянии и сплава в области перепассивации подтверждается найденными значениями энергии активации в растворе 2 н плавиковой плюс 6 н азотной кислот. [12]
Высказанные представления о молекулярной природе релаксационных переходов согласуются с мнением других авторов И-11 ], однако положения максимумов потерь и найденные значения энергии активации отличаются от ранее известных величин. Детальные обсуждения природы потенциальных барьеров в рассматриваемых полимерах были неизвестны. [13]
Этот результат подтверждает, что высокотемпературная модификация при охлаждении ниже 190 не превращается опять в низкотемпературную. Найденное значение энергии активации составляет 44 - 46 ккал-молъ-1. Общий характер кривых разложения, полученных Бартлеттом при температуре выше 190, аналогичен характеру кривых, полученных Одюбером. Хотя найденные этими авторами значения энергии активации и расходятся, величина скоростей и времен половинного разложения, приведенные ими, близки. [14]
Аноус, Брэдли и Колвин [114] критически рассмотрели ранее опубликованные данные по самоохлаждению; в более систематическом исследовании они показали что при начальной температуре 25 кристалл весом 1 г достигает устойчивого состояния в вакууме только через 40 мин. Эти данные по самоохлаждению-были использованы при вычислении скорости продвижения поверхности раздела в кристаллах с известной геометрией; найденные значения энергии активации составляют 22 8 и; 22 35 ккал-молъ-1, что расходится с результатами Купера ж Гарнера. [15]
Страницы: 1 2
