Двухвалентный свинец
Cтраница 1
Двухвалентный свинец может быть восстановлен в виде иодидного комплекса. С увеличением концентрации иодида потенциал полуволны смещается к более отрицательным значениям. На высоту волны концентрация KJ не влияет. [1]
Двухвалентный свинец определяется в растворах цитратов. NaOH ( pH приблизительно равен 8 5) можно определять до 0 0026 мг / мл РЬ. [2]
Одновременно положительно двухвалентный свинец РЬ за счет электронов генератора тока восстанавливается да металлического свинца, а ионы2Н ( из H2S04) с 804 -ионом ( из PbS04) образуют серную кислоту. [3]
Соединения двухвалентного свинца растворяются в конц. [4]
Карбонат двухвалентного свинца, РЬС03, встречается в природе в виде минерала церуссита. [5]
Ацетат двухвалентного свинца ( свинцовый сахар), РЬ ( СН3СОО) 2 - ЗН20, выделяется в процессе упаривания ( - 75) растворов окиси, гидроокиси или карбоната двухвалентного свинца в избытке уксусной кислоты. [6]
Ацетат двухвалентного свинца используют в текстильной промышленности как протраву. [7]
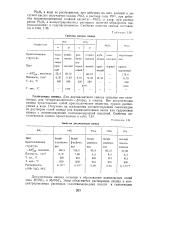 |
Свойства окислов свинца.| Свойства дигалогенидов свинца. [8] |
Для двухвалентного свинца описаны все гало-гениды, для четырехвалентного - фторид и хлорид. Все дигалогениды свинца представляют собой кристаллические вещества, трудно растворимые в воде. Получают их осаждением соответствующим галогенидом из растворов солей свинца или взаимодействием окиси или гидроокиси свинца с соответствующей галогенводородной кислотой. [9]
Для двухвалентного свинца известно всего несколько металлоорга-нических соединений. Наибольшее значение имеют тетраалкильные производные свинца. [10]
Соли двухвалентного свинца, как правило, плохо растворимы в воде. Эта соль имеет сладкий вкус, поэтому получила название свинцового сахара. Применяется при крашении тканей и для получения других соединений свинца. В отличие от солей двухвалентного олова соли свинца практически не обладают восстановительными свойствами. [11]
Образование двухвалентного свинца можно легко обнаружить. Для этого к полученному раствору в ту же пробирку следует прибавить одну каплю раствора иодида калия. Происходит выпадение осадка РЫ2, окрашенного в характерный желтый цвет. [12]
Образование двухвалентного свинца можно легко обнаружить. Для этого к полученному раствору в ту же пробирку следует прибавить одну каплю раствора иодида калия. Происходит выпадение осадка PbJ2, окрашенного в характерный желтый цвет. [13]
Образование двухвалентного свинца можно легко обнаружить. [14]
Соли двухвалентного свинца могут, так же как и соединения двухвалентного олова, окисляться до четырехвалентного состояния элемента. [15]
Страницы: 1 2 3 4