Свойство - литий
Cтраница 2
 |
Схема заполнения электронами энергетических уровней. [16] |
Электрон 3s связан с ядром слабее других и является валентным, или оптическим, электроном. В связи с этим химические и оптические свойства натрия подобны свойствам лития. [17]
Электрон 3s связан с ядром слабее других и является валентным или оптическим электроном. В связи с этим химические и оптические свойства натрия подобны свойствам лития. [18]
При переходе от лития Li к фтору F происходит закономерное ослабление металлических свойств и усиление неметаллических с одновременным увеличением валентности. Переход от фтора F к следующему по значению атомной массы элементу натрию Na сопровождается скачкообразным изменением свойств и валентности, причем натрий во многом повторяет свойства лития, будучи типичным одновалентным металлом, хотя в более активным. Как близкие родственники похожи друг на друга кремний Si и углерод С, фосфор Р и азот N, сера S и кислород О, хлор С1 и фтор F. При переходе к следующему за хлором в последовательности увеличения атомной массы элементу калию К опять происходит скачок в изменении валентности и химических свойств. Калий, подобно литию и натрию, открывает ряд элементов ( третий по счету), представители которого показывают глубокую аналогию с элементами первых двух рядов. [19]
При переходе от лития Li к фтору F происходит закономерное ослабление металлических свойств и усиление неметаллических с одновременным увеличением валентности. Переход от фтора F к следующему по значению атомной массы элементу натрию Na сопровождается скачкообразным изменением свойств и валентности, причем натрий во многом повторяет свойства лития, будучи типичным одновалентным металлом, хотя и более активным. Как близкие родственники похожи друг на друга кремний Si и углерод С, фосфор Р и азот N, сера S и кислород О, хлор С1 и фтор F. При переходе к следующему за хлором в последовательности увеличения атомной массы элементу калию К опять происходит скачок в изменении валентности и химических свойств. Калий, подобно литию и натрию, открывает ряд элементов ( третий по счету), представители которого показывают глубокую аналогию с элементами первых двух рядов. [20]
Например, когда сопоставлены были щелочные металлы с галоидами ( см. фотокопию I), то нельзя было еще заметить, что переход от фтора к натрию есть повторение свойств лития в общем ряду элементов, расположенных в единой последовательности по величине атомного веса. [21]
Расположение атомов в таких солеобразных гидридах напоминает расположение атомов в хлориде натрия. Их устойчивость уменьшается в том порядке, в котором выше перечислены элементы, причем гидрид лития гораздо более устойчив, чем остальные гидриды. Этот факт свидетельствует также о близком сходстве свойств лития и щелочноземельных металлов. [22]
Далее следует натрий Na ( ат. С водой реагирует весьма энергично, при этом выделяется водород и образуется щелочь. В соединениях натрий одновалентен. Натрий повторяет многие свойства лития. [23]
Переход количественных изменений в качественные совершается посредством постепенного исчезновения ( отрицания) предыдущих качеств. Так, во II периоде начиная с лития ( Li) в каждом последующем элементе постепенно исчезают ( отрицаются) некоторые из свойств предыдущего: бериллий ( Be) значительно менее металличен, чем литий, бор ( В) - чем бериллий, и так далее. У фтора ( F) наблюдается почти полное отсутствие ( отрицание) металличности, присущей элементам начала периода. При последующем же скачкообразном переходе от фтора через инертный газ неон ( Ne) к натрию ( Na), начинающему собой новый, III период, совершается отрицание отрицания, исчезают свойства фтора ( отрицающие свойства лития) и совершается возврат к свойствам лития, но уже на новой, высшей ступени их развития. Натрий еще более металличен, чем литий. Образно можно сказать, что литий в последующих за ним элементах II периода постепенно отмирает, чтобы вновь возродиться к жизни в форме натрия. [24]
Переход количественных изменений в качественные совершается посредством постепенного исчезновения ( отрицания) предыдущих качеств. Так, во II периоде начиная с лития ( Li) в каждом последующем элементе постепенно исчезают ( отрицаются) некоторые из свойств предыдущего: бериллий ( Be) значительно менее металличен, чем литий, бор ( В) - чем бериллий, и так далее. У фтора ( F) наблюдается почти полное отсутствие ( отрицание) металличности, присущей элементам начала периода. При последующем же скачкообразном переходе от фтора через инертный газ неон ( Ne) к натрию ( Na), начинающему собой новый, III период, совершается отрицание отрицания, исчезают свойства фтора ( отрицающие свойства лития) и совершается возврат к свойствам лития, но уже на новой, высшей ступени их развития. Натрий еще более металличен, чем литий. Образно можно сказать, что литий в последующих за ним элементах II периода постепенно отмирает, чтобы вновь возродиться к жизни в форме натрия. [25]
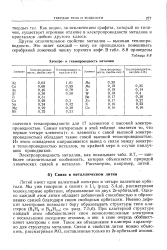 |
Электро - и теплопроводность металлов. [26] |
Литий имеет один валентный электрон и четыре валентные орби-тали. Мы уже говорили о связях в Li2 ( разд. Однако каждый атом лития обладает добавочной способностью к образованию связей благодаря своим свободным орбиталям. Именно дефицит электронов позволяет бору образовывать структуры типа кластеров ( В5Н9 и В10Н14; см. разд. При кластерной структуре каждый атом обобществляет свои немногочисленные электроны с несколькими соседними атомами, и они в свою очередь обобществляют электроны с ним. Такое же объединение в кластеры характерно для структуры металлов. Связи и свойства лития можно объяснить, рассматривая МО, составленные только из 25-орбиталей атомов. [27]
Страницы: 1 2