Свойство - щелочной металл
Cтраница 1
Свойства щелочных металлов, как видно из табл. 11, довольно правильно изменяются с увеличением атомного веса: повышается удельный вес, понижаются температуры плавления и кипения, усиливаются способность к отдаче электрона и щелочные свойства. [1]
Свойством щелочных металлов образовывать сильные щелочи и обусловлено их общее название. Почти все соли щелочных металлов хорошо растворимы в воде. В этом отношении составляют исключение LiCl, Li2CO3 и немногие другие. [2]
Какие свойства щелочных металлов характеризуют их как, наиболее типичные металлы. [3]
Какие свойства щелочных металлов характеризуют их как наиболее типичные металлы. [4]
Опишите коротко свойства щелочных металлов и расскажите о возможностях применения этих металлов. [5]
 |
Раство - Промышленное получение Na2SO4 и K2SO4 oc. [6] |
Из сопоставления свойств щелочных металлов и их соединений видно, что по ряду Li - Cs они в общем изменяются весьма закономерно. Подобно тому как это имело место у В и Be, первый элемент подгруппы - литий - занимает несколько особое положение. Малая растворимость его солей с анионами СОГ, РОГ и F, а также гидроокиси, сравнительная легкость отщепления от нее воды при нагревании и некоторые другие свойства приближают литий к магнию и кальцию. Однако в основном литий все же является типичным щелочным металлом. [7]
Из сопоставления свойств щелочных металлов и их соединений видно, что по ряду Li-Cs они в общем изменяются весьма закономерно. Подобно тому как это имело место у В и Be, первый элемент под группы - литий - занимает несколько особое положение. Малая растворимость его солей с анионами СОз -, Р0 - и F -, а также гидроокиси, сравнительная легкость отщепления от нее воды при нагревании и некоторые другие свойства приближают литий к магнию и кальцию. Однако в основном литий все же является типичным щелочным металлом. [8]
Из сопоставления свойств щелочных металлов и их соединений видно, что по ряду Li - Cs они в общем изменяются весьма закономерно. Подобно тому, как это наблюдалось у В и Be, первый элемент подгруппы - литий - занимает несколько особое положение. [9]
Различие в свойствах щелочных металлов состоит в степени их восстановительной активности. Наименее активным элементом среди них является литий. С увеличением атомного веса мет ал личность щелочных металлов возрастает и достигает максимума у франция. [10]
Аналогия в свойствах щелочных металлов обусловлена аналогией в структуре их внешнего электронного слоя. Таким образом, в настоящее время периодический закон, открытый Менделеевым, приобрел новый глубокий смысл - он стал отражением внутренней структуры атома. [11]
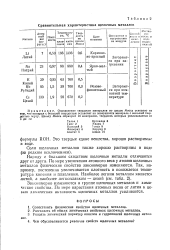 |
Сравнительная характеристика щелочных металлов. [12] |
Чем обусловливается различие свойств щелочных металлов. [13]
Рубидий и цезий имеют свойства щелочных металлов. Кристаллы алюмокалиевых квасцов характеризуются тем, что содержат определенные количества кристаллизационной воды и представляют форму октаэдрическую, очень характерную. И цезий и рубидий дают точно такие же двойные соли. [14]
Свойства растворов силикатов определяются свойствами щелочного металла ( К существенно отличается от Na, a Li близок по свойствам к Са2, особенно при температуре примерно 60 С), отношением SiCb / RaO ( модулем), концентрацией силиката щелочного металла. Концентрация SiCb в этих растворах ограничивается вязкостью ( растворы должны хорошо перекачиваться) и зависит от модуля. [15]
Страницы: 1 2 3 4