Свойство - белковая молекула
Cтраница 1
 |
Полиизобути-леновая цепь ( белые кружки - метильные группы. черные кружки - углеродные атомы цепи. [1] |
Свойства белковых молекул определяются частично общими свойствами полимеров с длинными цепями, частично-присутствием полярных амидных групп, а также свойствами боковых цепей. [2]
Как уже отмечалось, понимание структуры и свойств белковых молекул невозможно без учета их водного окружения ( см. гл. Рассмотрение ферментов в водном растворе как целостной системы необходимо и для изучения термодинамики ферментативных процессов. Такой системный подход характерен для методологии современной физики. Вычленение белковых молекул из окружающей их водной среды незакономерно в строгой теории. Это относится и к кинетике. Теория абсолютных скоростей реакций, переносящая на ферменты положения, справедливые для газовых реакций, пригодна лишь для грубых оценок. Теория ферментативных реакций требует учета физических свойств среды. [3]
Итак, боковыми цепями определяются в большой степени такие свойства белковой молекулы, как заряд, полярность, физические свойства, химическая активность, способность к гидратации, расщеплению ферментами и некоторые другие свойства. [4]
 |
Строение цепей главных валентностей целлюлозы ( а и крахмала ( б ( атомы кислорода заштрихованы. [5] |
Гидратация и сольватация белков приводит к изменению структуры и свойств белковой молекулы, что имеет большое значение в различных процессах взаимодействия белков с веществами среды. Сорбированные молекулы неэлектролитов вклиниваются между витками полипептидной цепи и разрывают водородные связи между ними. Гидратация белков влияет на вязкость их растворов. [6]
Гидратация и сольватация белков приводят к изменению структуры и свойств белковой молекулы, что имеет большое значение в различных процессах взаимодействия белков с веществами среды. Сорбированные молекулы неэлектролитов вклиниваются между витками полипептидной цепи и разрывают водородные связи между ними. Гидратация белков влияет на вязкость их растворов. [7]
Как известно, все многообразие жизненных форм обязано многообразию состава и свойств белковых молекул. Кроме биологической, белкам свойственна функциональная специфичность, отражающая функцию каждого белка в организме. [8]
Вместе с другими учеными советские физико-химики участвуют в решении ряда важнейших проблем современности: в изучении свойств белковых молекул, осуществлении управляемых термоядерных реакций, освоении атомной энергии, освоении космоса и недр Земли. [9]
Вместе с другими учеными советские физико-химики участвуют в решении ряда важнейших проблем современности: в изучении свойств белковых молекул, освоении атомной энергии, осуществлении управляемых термоядерных реакций, освоении космоса и недр земли. [10]
Хотя в ряде работ делались попытки количественной оценки степени гидрофобности и ее связи со структурой и свойствами белковых молекул [103- 115, 169, 184], вопрос о гидрофобной структуре белка далек от разрешения. Особенный интерес с этой точки зрения представляет исследование при постоянных рН и температурах солюбилизации гомологических рядов алифатических или ароматических углеводородов. [11]
Основан на снижении энергетич. Эти особенности обусловлены строением и свойствами белковой молекулы ферментов. В ней содержатся уникальные по своей структуре активные центры и регуляторные участки. Последовательные превращения реагентов осуществляются в составе фермент-субстратного комплекса по энергетически выгодному пути. Образование первичного фермент-субстратного комплекса дает выигрыш энергии, достаточный для ускорения процесса в целом. Представления о необходимости образования такого комплекса следовали из изучения зависимости скорости ферментативной реакции от концентрации фермента и субстрата, к-рая описывается в простейших случаях уравнением Михаэлиса - Ментен. [12]
Существует много методов и способов, с помощью которых ученые изучают белковую молекулу. Но теперь мы с вами уже более или менее ясно представляем себе, что в основном ученые знают о строении и свойствах белковой молекулы. [13]
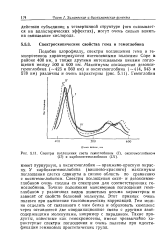 |
Спектры поглощения света гемоглобином ( /, оксигемоглобииом ( / / и карбоксигемоглобииом ( / / /. [14] |
У карбоксигемоглобина ( вишнево-красного) максимумы поглощения слегка сдвинуты в синюю область по сравнению с оксигемоглобином. Спектры поглощения окси - и дезоксимио-глобинов очень сходны со спектрами для соответствующих ге-моглобинов. Точные положения максимумов поглощения гемо-глобинов у различных видов животных весьма характерны и зависят от свойств белковой молекулы. Этот признак очень полезен при выяснении таксономических корреляций. Гем можно отделить от связанного с ним белка и образовать комплекс через оставшиеся две координационные связи с другими азотсодержащими молекулами, например с пиридином. Такие продукты, известные как гемохромогены, имеют чрезвычайно характерные спектры поглощения и очень полезны при идентификации геминовых простетических групп. [15]
Страницы: 1 2